hòa tan hoàn toàn 21,5g hỗn hợp hai kim loại A(hóa trị 1)và kim loại B(hóa trị 2) vào nước thu được 4,48 lít kí và dung dịch D. co cạn dung dịch D thu được chất rắn khan E
a) tính khối lượng chất rắn E
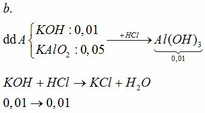
b)cũng lấy 21,5 g hỗn hợp hai kim loại trên tác dụng hết vs khí oxi ở nhiệt độ cao, thì thể tích khí oxi tác dụng vs kim loại A bằng lượng thể tích khí oxi tác dụng vs kim loại B. hỏi A,B la fkim loại nào trong K,Ca,Ba, Na,Li ? Biết hiệu suất pư xảy ra hoàn toàn và được đo ở đktc

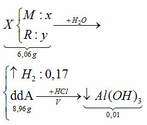
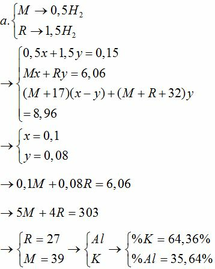


pthh :\(2A + 2H_20 \rightarrow 2AOH + H_2 \)
\(B+2H_2O \rightarrow B(OH)_2+H_2\)
\(n_{H_2}=\frac{4,48}{22,4}=0,2 (mol)\)
Ta thấy :
\(\sum n_{OH}=0,5.n_{H_2}\)
Mà \(n_{H_2}=0,2 (mol)\) \(\rightarrow \sum n_{OH}=0,1 (mol)\)
\(m_E=m_A+m_B+m_{OH}=21,5+0,1.17=23,2 (g)\)
b) Vì thể tích khí oxi tác dụng với kim loại A = lượng thể tích oxi tác dụng với kim loại B mà tỷ lệ thể tích bằng tỷ lệ số mol
Suy ra : số mol khí oxi tác dụng với kim loại A = số mol oxi tác dụng với kim loại B ( trong 21,5 g ) (1)
PTHH : \(4A+O_2->2A_2O\)
\(2B+O_2->2BO\)
Gọi số mol của A, B lần lượt là a, b
Từ (1) \(\rightarrow 0,25a=0,5b\) (*)
Vì khối lượng kim loại bằng 21,5 gam \(\rightarrow\)\(aA+bB=21,5 (g)\) (***)
Từ câu a, tác dụng với nước thu được 0,2 mol khí hidro \(\rightarrow 0,5a+b=0,2\) (**)
Giải phương trình (*)(**) : \(a=0,2 ; b=0,1\)
Thay vào (***) : \(0,2A+0,1B=21,5\)
Vì A và B > 0 \(\rightarrow A<\frac{21,5}{0,2}=107,5\)
Ta thử các trường hợp của A tương ứng với B
Vậy A là Kali và B là Bari