Tiến hành điện phân (có màng ngăn xốp ) 500ml dung dịch NaCl 4 M ( d= 1,2g/ml ) . Sau khí 75% NaCl bị điện phân thì dừng lại . Tính nồng độ phần trăm của các chất trong dung dịch sau khi điện phân.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn đáp án B
Ta có:
![]()
![]()
BTNT.Clo → Khí thoát ra ở cực dương phải là Cl2 và O2 .
Ta có
![]()
![]()
Và
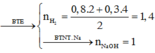
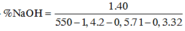
=7,96%

Đáp án A
mdung dịch = 200.1,1 = 220 (g); nNaOH = nNaCl = 0,2.2 = 0,4 (mol)
dễ thấy khí thoát ra ở catot là H2 với = 1 (mol)


Chọn A.
Vì dung dịch sau phản ứng hòa tan được CuO -> Có H+
Ta có n(H+ = 2n(CuO) = 0,08 mol -> n(O2) = n(H+/4) = 0,02
Mà n(Cl2) + n(O2) = 0,04 -> n(Cl2) = 0,02 mol
Áp dụng định luật bảo toàn nguyên tố Clo -> n(NaCl) = 2n(NaCl) = 0,04 mol
Áp dụng định luật bảo toàn mol e: n(CuSO4) = 4n(O2) + 2n(Cl2))/2 = 0,06
-> m = 0,06∙160 + 0,04∙58,5 = 11,94 gam

Đáp án A
Vì dung dịch sau phản ứng hòa tan được CuO → có H+
+ Ta có nH+ = 2nCuO = 0,08 mol ⇒ nO2↑ = nH+/4 = 0,02 mol
Mà nCl2 + nO2 = 0,04 ⇒ nCl2 = 0,02 mol
+ BT nguyên tố clo ⇒ nNaCl = 2nNaCl = 0,04 mol
BTe ta có nCuSO4 = (4nO2 + 2nCl2) ÷ 2 = 0,06 mol
→ m = 0,06×160 + 0,04×58,5 = 11,94 gam

Đáp án A
Vì dung dịch sau phản ứng hòa tan được CuO → có H+
+ Ta có nH+ = 2nCuO = 0,08 mol ⇒ nO2↑ = n H + 4 = 0,02 mol
Mà nCl2 + nO2 = 0,04 ⇒ nCl2 = 0,02 mol
+ BT nguyên tố clo ⇒ nNaCl = 2nNaCl = 0,04 mol
BTe ta có nCuSO4 = (4nO2 + 2nCl2) ÷ 2 = 0,06 mol
→ m = 0,06×160 + 0,04×58,5 = 11,94 gam

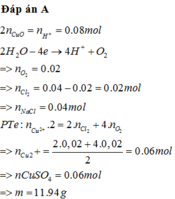
Đổi : 500ml = 0,5 l
n NaCl = 4 . 0,5 = 2 mol
\(\Rightarrow\) m NaCl bị điện phân = 2 . 75% = 1,5 mol
2NaCl + 2H2O \(\rightarrow\) 2NaOH + H2 + Cl2
1,5............................1,5........0,75.....075
m dd NaCl = 500 . 1,2 = 600 g
m dd sau pứ = m dd NaCl - m H2 - m Cl2
= 600 - 0,75 . 2 - 0,75 . 71 = 545,25 g
m NaOH = 0,75 . 40 = 30 g
C% NaOH = \(\dfrac{30}{545,25}\).100% = 5,5 %
sao n NaCl = 1,5 v ạ , giải thích rõ hơn đc k