Nung nóng Kali nitrat KNO3,chất này bị phân hủy thành kali nitrat KNO2 và oxi O2. biết hiệu suất của phản ứng đạt 8,5%theo lý thuyết
1/tính khối lượng KNO3 cần dùng để điều chế được 2,4g oxi
2/Tính khối lượng khí oxi thu được khí phân hủy 10,1g KNO3
giúp mk nha mai mk phải nộp rùi.thanks

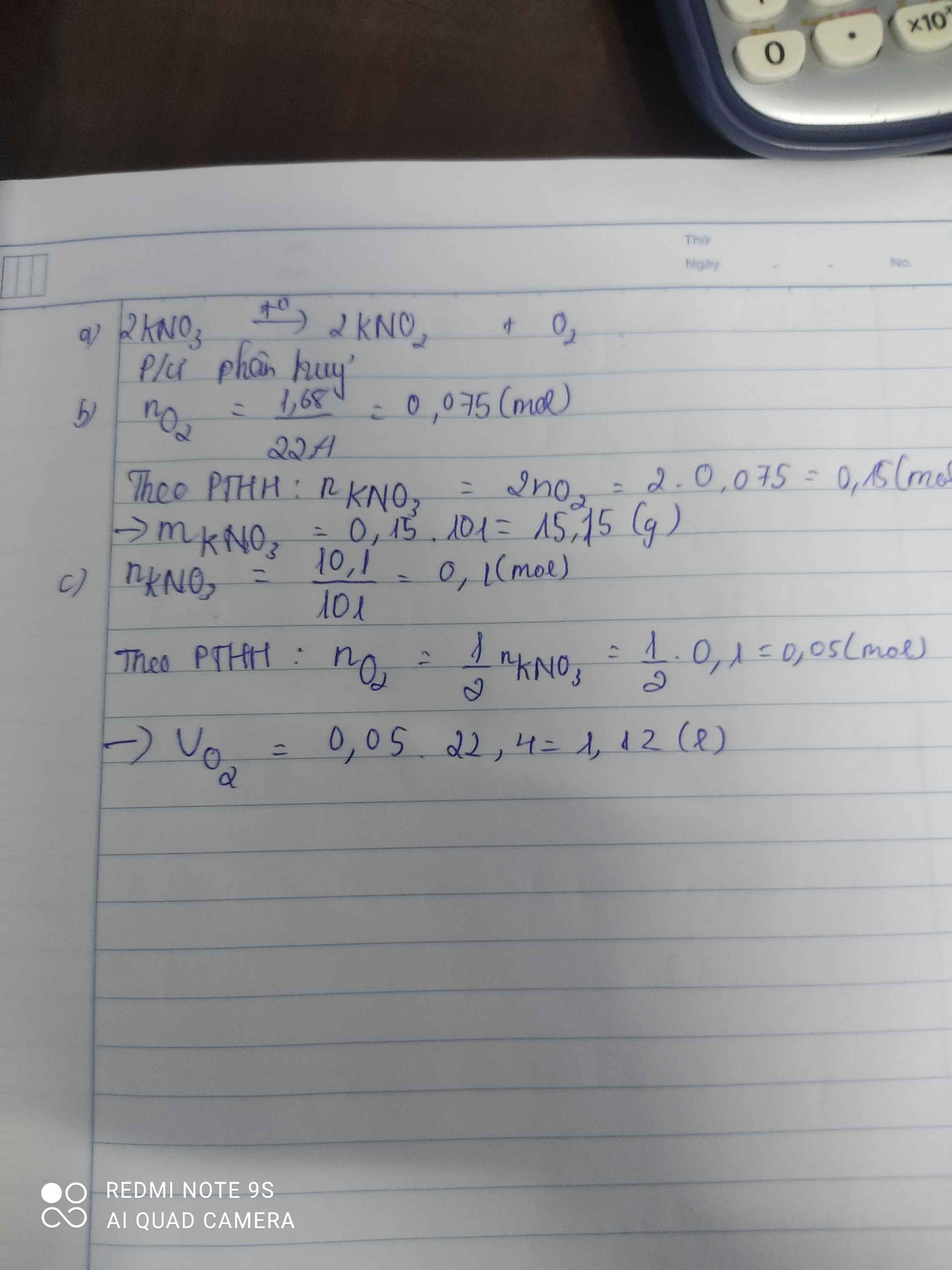
PTHH:
2KNO3 \(\rightarrow\) 2KNO2 + O2
1/ Số mol của 2,4 g O2 là:
2,4 : 32 = 0,075 (mol)
Theo PTHH, số mol KNO3 cần dùng là 0,075 . 2 = 0,15 (mol)
Khối lượng KNO3 cần dùng là:
0,15 (39+14+16.3) = 15,15 (g)
Vì hiệu suất phản ứng là 8,5% nên khối lượng KNO3 thực cần dùng là:
15,15 : (100-8.5) . 100 = 16,56(g)
2/ Khối lượng KNO3 phân húy là:
10,1 : (39+14+16.3) = 0,1 (mol)
Theo PTHH, số mol O2 thu được là: 0,1 : 2 = 0,05 (mol)
Khối lượng khí O2 thu được là:
0,05 . 32 = 1,6 (g)