Cho bản sắt có khối lượng 100 gam vào 2 lít dung dịch CuSO4 1M. Sau một thời gian dung dịch CuSO4 có nồng độ là 0,8 M. Tính khối lượng bản kim loại, biết rằng thể tích dung dịch xem như không đổi và khối lượng đồng bám hoàn toàn vào bản sắt ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, Cứ 1 mol sắt tan trong dd thì sẽ có 1 mol Cu bám vào thanh sắt ⇒ Khối lượng tăng 8g
Vậy khi khối lượng tăng 0,8g thì nCu = nFe = 0.1 (mol)
⇒ mCu trên thanh sắt = 6,4 (g)
b, Các chất tan trong A: CuSO4; FeSO4
V = 500 ml = 0,5 (l)
nCuSO4 ban đầu = 0,5 (mol)
nCuSO4 phản ứng = 0,1 (mol)
⇒ nCuSO4 trong dd = 0,4 (mol)
⇒ CMCuSO4 = 0.8 (M)
nFeSO4 = nFe = 0,1 (mol)
⇒ CMFeSO4 = 0,2 (M)
PTHH: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
a) Gọi số mol Fe phản ứng là \(x\) \(\Rightarrow n_{Cu}=x\left(mol\right)\)
Ta có: \(64x-56x=0,8\) \(\Leftrightarrow x=0,1\)
\(\Rightarrow m_{Cu\left(bámvào\right)}=0,1\cdot64=6,4\left(g\right)\)
b) Ta có: \(n_{CuSO_4}=0,5\cdot1=0,5\left(mol\right)\)
\(\Rightarrow n_{CuSO_4\left(dư\right)}=0,5-0,1=0,4\left(mol\right)\)
Mặt khác: \(n_{FeSO_4}=0,1mol\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{CuSO_4}}=\dfrac{0,4}{0,5}=0,8\left(M\right)\\C_{M_{FeSO_4}}=\dfrac{0,1}{0,5}=0,2\left(M\right)\end{matrix}\right.\)

$n_{CuSO_4} = 2(mol)$
$n_{CuSO_4\ dư} = 2.0,8 = 1,6(mol)$
$\Rightarrow n_{CuSO_4\ pư} = 2 - 1,6 = 0,4(mol)$
$Fe + CuSO_4 \to FeSO_4 + Cu$
Theo PTHH :
$n_{Fe} = n_{CuSO_4\ pư} = 0,4(mol)$
$m_{Fe} = 0,4.56 = 22,4(gam)$


Theo (1) có khối lượng Cu bám vào: mCu = 0,4.2,5.64 = 64 (gam)
Theo (2) có khối lượng Cu bám vào: mCu = 0,4.64 =25,6 (gam).
Đáp án A

trên mạng mk thấy có một bài tượng tự trên hocmai, bạn vào đó tham khảo nhé
Nhưng mà bài đó không phải là tính số mol mà tính nồng độ phần trăm mình xem bài đó rồi bạn

Đáp án : A
Khi cho Fe vào thấy khối lượng kim loại thu được tăng => Còn Cu2+
+) Catot : Cu2+ + 2e -> Cu
,a -> 2a -> a
+) Anot : 2H2O – 4e -> 4H+ + O2
,2a -> 2a -> 0,5a
=> mgiảm = 4 = mCu pứ + mO2 = 64a + 16a => a = 0,05 mol
Dung Dịch sau điện phân có b mol Cu2+ và 0,1 mol H+
=> mKL sau – mKl trước = mCu – mFe pứ = 64b – 56.( b + 0,1.0,5) = 38,2 – 36,4
=> b = 0,575 mol
=> x = 1,25M

Ta có: \(n_{Fe}=\dfrac{3,92}{56}=0,07\left(mol\right)\)
\(PTHH:Fe+CuSO_4--->FeSO_4+Cu\downarrow\)
a. Theo PT: \(n_{Cu}=n_{FeSO_4}=n_{Fe}=0,07\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,07.64=4,48\left(g\right)\)
Ta có: \(V_{dd_{FeSO_4}}=V_{dd_{CuSO_4}}=\dfrac{200}{1000}=0,2\left(lít\right)\)
\(\Rightarrow C_{M_{FeSO_4}}=\dfrac{0,07}{0,2}=0,35M\)
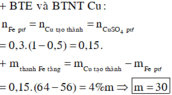

nCuSO4 = V * C (M) = 2*1 = 2 (mol)
n CuSO4 sau khi phản ứng là = V * C(M 2) = 2*0,8 = 1,6 (mol)
Fe + CuSO4 - > FeSO4 + Cu
0,4 <- 0,4-> 0,4 mol ----> 0,4 mol
m Fe phản ứng = n * M =0,4 *56=22,4 (g)
m Cu sinh ra là =n*M =0,*4*64=25,6(g)
m Fe còn lại là = m Fe ban đầu - m Fe phản ứng = 100-22,4 =77,6 (g)
m bản kim loại = m Fe còn lại + m Cu sinh ra = 77,6 +25,6= 103,2 (g)
có gì sai mong mọi người sửa giùm em nha !
nCuSO4 = V * C (M) = 2*1 = 2 (mol)
n CuSO4 sau khi phản ứng là = V * C(M 2) = 2*0,8 = 1,6 (mol)
Fe + CuSO4 - > FeSO4 + Cu
0,4 <- 0,4-> 0,4 mol ----> 0,4 mol
m Fe phản ứng = n * M =0,4 *56=22,4 (g)
m Cu sinh ra là =n*M =0,*4*64=25,6(g)
m Fe còn lại là = m Fe ban đầu - m Fe phản ứng = 100-22,4 =77,6 (g)
m bản kim loại = m Fe còn lại + m Cu sinh ra = 77,6 +25,6= 103,2 (g)