Nung 2 tấn CaCO3 -> CaO và CO2. Tính mCaO biết hiệu suất phản ứng là 90%.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(300kg=300000g\)
\(CaCO3-->CaO+CO2\)
\(n_{CaCO3}=\frac{300000}{100}=3000\left(mol\right)\)
\(n_{CaO}=n_{CaCO3}=3000\left(mol\right)\)
\(m_{CaO}=3000.56=168000\left(g\right)=168\left(kg\right)\)
Mk nghĩ đề là 134,4 kg ý
\(H\%=\frac{134,4}{168}.100\%=80\%\)
b) \(CaCO3-->CaO+CO2\)
\(1tấn=1000000g\)
\(n_{CaCO3}=\frac{1000000}{100}=10000\left(mol\right)\)
\(n_{CaO}=n_{CaCO3}=10000\left(mol\right)\)
\(m_{CaO}=10000.56=560000\left(g\right)=0,56\left(tấn\right)\)
Do H%=90%
\(\Rightarrow m_{CaO}=0,56.90\%=0,504\left(tấn\right)\)
c) \(7,84tấn=7840000\left(kg\right)\)
\(n_{CaO}=\frac{78400000}{56}=1400000\left(mol\right)\)
\(CaCO3-->CaO+CO2\)
\(n_{CaCO3}=n_{CaO}=1400000\left(mol\right)\)
\(m_{CaCO3}=1400000.100=140000000\left(g\right)=14tấn\)
a) CaCo3 \(\underrightarrow{t^o}\) CaO + Co2
3 -> 3 -> 3 /mol
nCaCo3 = \(\frac{300}{100}=3\left(mol\right)\)
\(m_{CaOpt}\) = 3.56 = 168 (g)
H = \(\frac{134,4}{168}.100\%=80\%\)
b) Giả sử nung 1 tấn CaCo3 là nung 1g CaCo3
CaCo3 \(\underrightarrow{t^o}\) CaO + Co2
0,01 -> 0,01 -> 0,01 /mol
nCaCo3 = \(\frac{1}{100}=0,01\left(mol\right)\)
mCaOpt = 0,01.56 = 0,56 (g)
mCaOtt = 0,56.90% = 0,504 (g)
Vậy thu được 0,504 tấn CaO khi nung 1 tấn CaCo3 với hiệu suất 90%
c) Giả sử 7,84 tấn CaO là 7,84 g CaO
CaCo3 \(\underrightarrow{t^o}\) CaO + Co2
0,098 <- 0,098 /mol
mCaOpt = 7,84.70% = 5,488 (g)
nCaO = \(\frac{5,488}{56}=0,098\left(mol\right)\)
mCaCo3 = 0,098.100 = 9,8 (g)
Vậy cần dùng 9,8 tấn CaCo3 để sau phản ứng thu đc 7,84 tấn CaO với hiệu suất 70%

\(n_{CaO} = \dfrac{11,2.1000}{56} = 200(kmol)\\ CaCO_3 \xrightarrow{t^o} CaO + CO_2\\ n_{CaCO_3\ pư} = n_{CaO} = 200(kmol)\\ n_{CaCO_3\ đã\ dùng} = \dfrac{200}{80\%} = 250(kmol)\\ m_{CaCO_3} = 250.100 = 25000(kg)\\ \Rightarrow m_{đá\ vôi} = \dfrac{25000}{90\%} = 27777,78(kg)\)

15 tấn = 15 000(kg)
$m_{CaCO_3} = 15000.90\% = 13500(kg)$
$n_{CaCO_3} = \dfrac{13500}{100} = 135(kmol)$
$n_{CaCO_3\ pư} = 135.85\% = 114,75(kmol)$
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
Theo PTHH : $n_{CaO} = n_{CaCO_3} = 114,75(kmol)$
$m_{CaO} = 114,75.56 = 6426(kg)$
Giải đáp thắc mắc :
100 là phân tử khối của $CaCO_3$
56 là phân tử khối của $CaO$
Cách làm như ảnh trên là áp số tỉ lệ về khối lượng theo PTHH

mCaO=5,6(tấn)= 5600000(g)
=>CaO= 5600000/56=100000(mol)
PTHH: CaCO3 -to-> CaO + CO2
nCaCO3(LT)=nCaO=100000(mol)
Vì H=80% => nCaO(TT)= 100000: 80%= 125000(mol)
=> mCaCO3=125 000 . 100 = 12 500 000(g)= 12,5(tấn)
=>m(đá vôi)=12,5 : 90%=13,889(tấn)
Chúc em học tốt!

nCaO = 5,6/56 = 0,1 (mol)
PTHH: CaCO3 -> (to) CaO + CO2
Mol: 0,1 <--- 0,1 <--- 0,1
nCaCO3 (bđ) = 14/100 = 0,14 (mol)
H = 0,1/0,14 = 71,42%
nCaCO3 = 14: 100 =0,14 (mol)
nCaO = 5,6 : 56= 0,1
pthh ; CaCO3 -t--> CaO + CO2
0,14---------->0,14(mol)
ta có
mCaO (tt ) = 0,1 . 56 = 5,6 (g)
mCaO lt = 0,14.56 =7,84(g)
H%=(mCaOtt : mCaOlt ) . 100 %
= (5,6 : 7,84 ) .100%=71,42 %

1)
1,2 tấn = 1200(kg)
5 tạ = 500(kg)
mCaCO3=1200.80%=960(kg)mCaCO3=1200.80%=960(kg)
CaCO3to→CaO+CO2nCaCO3 pư=nCaO=50056(mol)⇒H=50056.100960.100%=93%
\(m_{\text{CaCO_3}}=1000.95\%=950kg\\ \rightarrow n_{\text{CaCO_3}}=9,5mol\)
\(m_{CaCO_3}\underrightarrow{t^o}CaO+CO_2\)
9,5 → 9,5
\(\rightarrow V_{CO_2}=9,5.22,4=212,8\)
→ hiệu suất phản ứng là
\(\dfrac{159,6}{212,8}.100=75\%\)

mCaCO3 = 500*80%= 400 (g)
nCaCO3 = 400/100 = 4 (mol)
nCaCO3(pư) = 4*70%=2.8 (mol)
CaCO3 -to-> CaO + CO2
2.8..................2.8
Chất rắn X : CaCO3 dư , CaO
mX = ( 4 -2.8 ) *100 + 2.8*56 = 276.8 (g)
%CaO = 2.8*56/276.8 * 100% = 56.64%
a)mCaCO3=500.80%=400(g) -> nCaCO3=400/100=4(mol)
PTHH: CaCO3 -to-> CaO + H2O
nCaO(LT)=nCaCO3=4(mol)
=> nCaO(TT)=4. 70%=2,8(mol)
=>mX=mCaO+ m(trơ)+ mCaCO3(chưa p.ứ)=2,8.56+100+ 1,2.100=376,8(g)
b) %mCaO= (156,8/376,8).100=41,614%
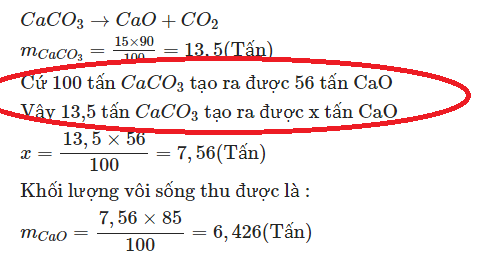
Đổi 2 tấn = 2000 kg.
Gọi mCaO = x kg.
Ta có pt \(\dfrac{2000}{100}=\dfrac{x}{60}\)
Suy ra x = 2000*60/100 = 1200 kg.
Ta có H = 90 phần trăm.
Suy ra mCaO thực tế = 1200*90/100 = 1080 kg.