1.dung dịch A chứa 0,2 mol Na2CO3 và 0,3mol NaHCO3,dung dịch B chứa 0,5 mol HCl
TN1:Đổ rất từ từ B vào A cho đến hết
TN2:Đổ rất từ từ A vào B cho đến hết
TN3:Trộn nhanh 2 dd A và B với nhau
Tính thể tích khí bay ra trong 3 thí nghiệm trên
2.Khi cho a gam Fe vào trong 400ml dd HCl.Sau pứ đem cô cạn dd thu được 6,2g rắn X.Nếu cho hỗn hợp gồm a gam Fe và b gam Mg vào trong 400ml dung dịch HCl thì sau pứ thu được 896ml H2 và cô cạn dung dịch thu được 6,68g rắn Y
Tính a,b nồng độ phân tử gam của dung dịch HCl và thành phần khối lượng các chất trong X,Y(giả sử Mg không pứ với nước và khi pứ với axit thì Mg pứ trước hết với axit rồi mới đến Fe.Các pứ xảy ra hoàn toàn)

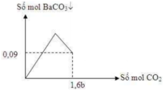

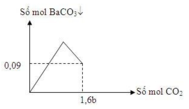
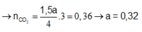
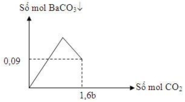
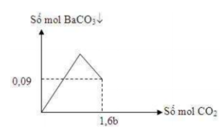
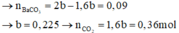
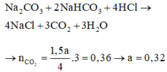


2/ Giả sử Fe phản ứng hết:
\(\Rightarrow n_{FeCl_2}=\dfrac{6,2}{127}=0,0488\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2\left(0,0488\right)+H_2\left(0,0488\right)\)
Số mol H2 trong phản ứng 2: \(\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
Ta nhận xét: Khối lượng lúc sau hơn lúc đầu phần Mg nhưng mà số mol H2 lại ít hơn chứng tỏ trong phản ứng đầu Fe đư. Và số mol của H2 chính là số mol của H2 ở thí nghiệm 1 là 0,04 (mol).
\(Fe\left(0,04\right)+2HCl\rightarrow FeCl_2\left(0,04\right)+H_2\left(0,04\right)\)
\(\Rightarrow a-56.0,04+127.0,04=6,2\)
\(\Leftrightarrow a=3,36\left(g\right)\)
Giả sử chỉ có phản ứng Mg với HCl thì khối lượng tối thiểu chất rắn sau phản ứng là:
\(Mg+2HCl\rightarrow MgCl_2\left(0,04\right)+H_2\left(0,04\right)\)
\(\Rightarrow m_r=3,36+0,04.95=7,16\left(g\right)>6,68\left(g\right)\)
\(\Rightarrow Fe\) có tham gia phản ứng.
Gọi số mol của Fe, và Mg tham gia phản ứng lần lược là x, y thì ta có:
\(Fe\left(x\right)+2HCl\rightarrow FeCl_2\left(x\right)+H_2\left(x\right)\)
\(Mg\left(y\right)+2HCl\rightarrow MgCl_2\left(y\right)+H_2\left(y\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x+y=0,04\\3,36+71x+95y=6,68\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,02\end{matrix}\right.\)
Làm nốt nhá
sao số mol H2 ở thì nghiệm 1 lại là 0,04 vậy a