Dẫn 3,36 lit khí HCl (đktc) vào 100 ml dung dịch AgNO3 8% (d = 1,1 g/ml) thu được dung dịch X. Nồng độ % của axit nitric trong dung dịch X là:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nMnO2=69,6/87=0,8 mol
MnO2 +4 HCl =>MnCl2 +Cl2 +2H2O
0,8 mol =>0,8 mol
khí X là Cl2
VCl2=0,8.22,4=17,92 lit
nNaOHbđ=0,5.4=2 mol
Cl2 +2NaOH =>NaCl +NaClO +H2O
0,8 mol=>1,6 mol=>0,8 mol=>0,8 mol
dư 0,4 mol
CM dd NaOH dư=0,4/0,5=0,8M
CM dd NaCl=CM dd NaClO=0,8/0,5=1,6M
0,8 mol

Chọn đáp án A
Do VCO2 ở 2 thí nghiệm khác nhau ⇒ HCl không dư || nHCl = 0,1x; nCO32– = 0,1y mol; nHCO3– = 0,2y mol.
Thí nghiệm 1: nCO2 = nH+ - nCO32– = 0,1x - 0,1y
Thí nghiệm 2: do ban đầu nHCO3– = 2.nCO32– ⇒ nHCO3– phản ứng = 2.nCO32–phản ứng
⇒ nCO32–phản ứng = 0,1x ÷ (2 + 2 × 1) = 0,025x ⇒ nHCO3– phản ứng = 0,05x ⇒ nCO2 = 0,025x + 0,05x = 0,075x
⇒ 0,075x = 2 × (0,1x - 0,1y) ⇒ 0,125x = 0,2y ⇒ x : y = 8 : 5 ⇒ chọn A.
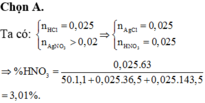
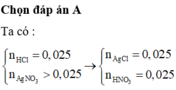
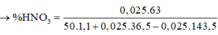

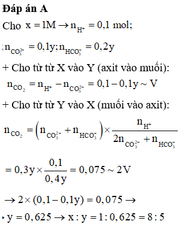
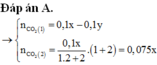
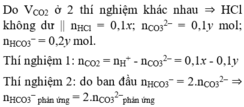

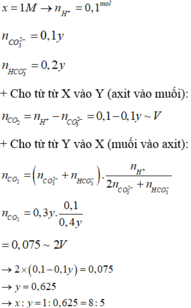
\(n_{HCl}=\dfrac{3,36}{22,4}=0,15\left(mol\right);n_{AgNO_3}=\dfrac{100.1,1.8\%}{170}=\dfrac{22}{425}\left(mol\right)\)
\(AgNO_3+HCl\rightarrow AgCl+HNO_3\)
Lập tỉ lệ: \(\dfrac{22}{425}< \dfrac{0,15}{1}\Rightarrow\)Sau phản ứng HCl dư
\(n_{HNO_3}=n_{AgNO_3}=\dfrac{22}{425}\left(mol\right)\\ m_{ddsaupu}=0,15.36,5+100.1,1-\dfrac{22}{425}.143,5=108,05\left(g\right)\)
\(C\%_{HNO_3}=\dfrac{\dfrac{22}{425}.63}{108,5}.100=3,02\%\)