Cho kim loại A tác dụng với dung dịch AgNO3 dư .Lượng chất răn kết tủa thu được gấp 12 lần khối lượng kim loại A đem phản ứng .
a, Xác định kim loại A
b, Nếu cho A tác dụng với dd FeCl3 theo tỉ lệ mol 1:2 thì sau phản ứng hoàn toàn , khối lượng chất rắn thu được gấp bao nhiêu lần khối lượng A







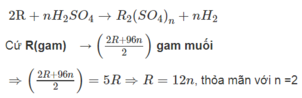
 = 0,75
= 0,75
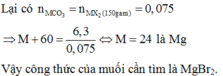
Gọi n là hóa trị của A ; \(1\le n\le3\)
Gọi x là số mol của A
\(A+nAgNO_3\rightarrow A\left(NO_3\right)_n+nAg\downarrow\)
x -----------------------------------> xn
theo gt: \(m_{Ag}=12m_A\)
\(\Leftrightarrow108xn=12.xM_A\)
\(\Rightarrow M_A=9n\)
Kẻ bảng.. => n =3 thì MA = 27 ( nhận )
A là Al
\(Al+FeCl_3\rightarrow AlCl_3+Fe\)
x --------------------------> x
\(\dfrac{m_{Fe}}{m_{Al}}=\dfrac{56x}{27x}=2,07\)
=> \(m_{Fe}=2,07m_{Al}\)
\(1\le n\le3\)
loại loại nhận
Đối với những ẩn như vậy thì lập bảng ra.