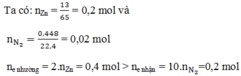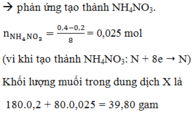Hòa tan hoàn toàn 4,29 gam 2 kl X,Y ở 2 chu kỳ liên tiếp và thuộc nhóm IA trong nc(dư), thu đc 3,024l khí H2(Đktc). 2 kl XY là??
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 1 . Gọi CT của oxit là R2On (n là hóa trị của R)
\(R_2O_n+nH_2\rightarrow2R+nH_2O\)
0,06/n<-----0,08
=> \(\dfrac{13,38}{2R+16n}=\dfrac{0,06}{n}\)
n=1 => R=103,5 (loại)
n=2 => R=207 (Pb)
n=3 => R=310,5 (loại)
Vậy kim loại cần tìm là Pb
2. \(A+2HCl\rightarrow ACl_2+H_2\)
\(B+2HCl\rightarrow BCl_2+H_2\)
Ta có : \(n_A=n_B=\dfrac{1}{2}\Sigma n_{H_2}=0,1\left(mol\right)\)
Ta có : \(0,1.M_A+0,1.M_B=8,9\)
=> \(M_A+M_B=89\)
Xét bảng sau:
| A | 24 | 40 | 56 | 137 |
| B | 65 | 49 | 33 | / |
Vậy A là Mg và B là Zn

PTHH: 2Al + 3H2SO4 \(\rightarrow\)Al2(SO4)3 + 3H2\(\uparrow\)
Theo pt: . 2 ........ 3................... 1............ 3.... (mol)
Theo đề: 0,2 ..... 0,3 ............... 0,1 ........ 0,3... (mol)
a) \(n_{Al}=\dfrac{m}{M}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(V_{H_{2_{đktc}}}=n.22,4=0,3.22,4=6,72\left(l\right)\)
b) \(m_{Al_2\left(SO_4\right)_3}=n.M=0,1.342=34,2\left(g\right)\)
c)
Cách 1:
\(m_{H_2}=n.M=0,3.2=0,6\left(g\right)\)
Theo định luật bảo toàn khối lượng, ta có:
mAl + m H2SO4 = mAl2(SO4)3 + mH2
=> mH2SO4 = mAl2(SO4)3 + mH2 - mAl = 34,2 + 0,6 - 5,4 = 29,4 (g)
Cách 2:
mH2SO4 = n.M = 0,3.98 = 29,4 (g)
Cô bổ sung 1 chút ở cách 2: Nên thêm nH2SO4=nH2=0,3mol

Đáp án C
Ta có:
![]()
ne nhường = 2.nZn = 0,4 mol > ne nhận = 10.nN2 = 0,2 mol → phản ứng tạo thành NH4NO3.
![]()
(vì khi tạo thành NH4NO3: N + 8e → N)
Khối lượng muối trong dung dịch X là = 180.0,2 + 80.0,025 = 39,80 gam
Lưu ý: Đề bài không nói thu được khí X duy nhất nên có thể có muối NH4NO3 tạo thành.

Đáp án C
Ta có:
![]()
ne nhường = 2.nZn = 0,4 mol > ne nhận = 10.nN2 =0,2 mol → phản ứng tạo thành NH4NO3.
![]()
(vì khi tạo thành NH4NO3: N + 8e → N)
Khối lượng muối trong dung dịch X là = 180.0,2 + 80.0,025 = 39,80 gam

a) Zn + 2HCl --> ZnCl2 +H2 (1)
2Al + 6HCl --> 2AlCl3 +3H2 (2)
nH2 = 8,512/22,4=0,38(mol)
=> mH2=0,38 .2=0,76(g)
theo PTHH : nHCl=2nH2=0,76(mol)
=> mHCl=0,76.36,5=27,74(g)
áp dụng định luật bảo toàn khối lượng ta có :
mmuối=16,24+27,74-0,76=43,22(g)
b) giả sử nZn =x(mol)
nAl=y(mol)
=>65x+27y=16,24 (I)
theo (1) : nH2=nZn =x(mol)
theo(2) : nH2 =nAl=y(mol)
=> 2x + 2y=0,76(II)
từ (I) và (II) ta có :
65x+27y=16,24
2x+2y=0,76
=>x=0,15(mol)
y=0,22(mol)
=> mZn =0,15.65=9,75(g)
mAl=16,24 - 9,75=6,49(mol)
=>%mZn=9,75/16,24 .100=60,03%
%mAl=100 - 60,03=39,96%
c) theo pthh : nHCl=nZn,Al=0,15+0,22=0,37(mol)
=>mHCl=0,37.36,5=13,505(g)

Đáp án D
Ta có: = 0,145 mol
Quy đổi 20,88 g oxit sắt FexOy thành 20,88 g Fe và O
Gọi nFe = x mol; nO = y mol
Quá trình nhường electron:
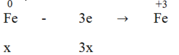
Quá trình nhận electron:
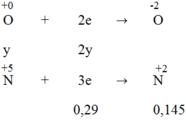
Áp dụng định luật bảo toàn electron, ta có:
3x = 2y + 0,29 → 3x - 2y = 0,29 (1)
Mặt khác: 56x + 16y = 20,88 (2)
Từ (1) và (2) → x = 0,29 và y = 0,29
Muối sinh ra là muối Fe2(SO4)3. Áp dụng ĐL bảo toàn nguyên tố ta có:
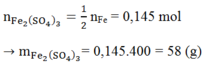

Đáp án C
Ta có: nCO = 0,8 mol; = 0,9 mol
Gọi n là hóa trị của kim loại M (1 ≤ n ≤ 3)
Trong phản ứng giữa M với H2SO4 đặc nóng, M là chất khử nhường electron.
H2SO4 đặc là chất oxi hóa nhận electron:

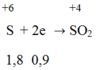
Trong phản ứng khử oxit kim loại bởi CO ta luôn có:
nO (trong oxit) = nCO = 0,8 mol
⇒Tỉ lệ:
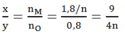
Dựa vào các đáp án ta thấy n = 2 hoặc n = 3