Hỗn hợp X khối lượng 14,46 gam gồm Al và Fe2O3. Thực hiện phản ứng nhiệt nhôm hoàn toàn thu duopcwj hỗn hợp Y. Chia Y thành 2 phần:
- Phần 1: Hòa tan trong dung dịch NaOH dư thu được 0.672 lít H2
- Phần 2: hòa tan trong dung dịch axit H2SO4 loãng dư thu đucợ 3,136 lít khí H2. tính khói lượng của Al trong X



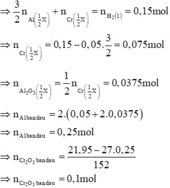



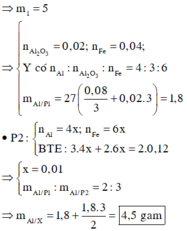


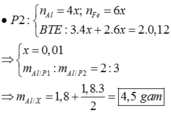


2Al + Fe2O3 -> Al2O3 + 2Fe (1)
2Al + 2NaOH + 2H2O -> 2NaAlO2 + 3H2 (2)
Al2O3 + 2NaOH -> 2NaAlO2 + H2O (3)
Fe + H2SO4 -> FeSO4 + H2 (4)
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2 (5)
Al2O3 + 3H2SO4 -> Al2(SO4)3 + 3H2O (6)
*Trong mỗi phần:
nH2(PI)=0,03(mol)
nH2(PII)=0,14(mol)
Theo PTHH 2 ta có:
\(\dfrac{2}{3}\)nH2=nAl dư=0,02(mol)
Theo PTHH 5 ta có:
nH2(5)=\(\dfrac{3}{2}\)nAl dư=0,03(mol)
nH2(4)=0,14-0,03=0,11(mol)
Theo PTHH 4 ta có:
nH2=nFe=0,11(mol)
Theo PTHH 1 ta có:
nFe=nAl(1)=0,11(mol)
=>\(\sum\)nAl=0,11+0,02=0,13(mol)
mAl trong mỗi phần=27.0,13=3,51(g)
mAl trong X=3,51.2=7,02(g)
umk chắc thế Đỗ Quang Duy