1. Hợp chất A được tạo thành từ ion M+ và ion X2- (được tạo ra từ các nguyên tố M và X tương ứng). Trong phân tử A có tổng số các hạt cơ bản là 140 trong đó số hạt mang điện bằng 65.714% tổng số hạt. Số khối của M lớn hơn của X là 23. Nguyên tố M là?
2. Nguyên tố X có 2 đồng vị bền X1, X2. Tổng số hạt trong 2 nguyên tử đông vị X1, X2 là 106. Biết đồng vị X1 có số hạt Nơtron nhiều hơn số hạt Proton là 1. Xác định số khối của 2 đồng vị trên.
Cảm ơn mọi người trước 😀😀


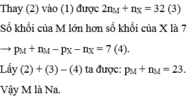
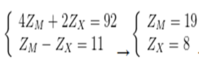

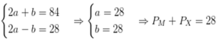
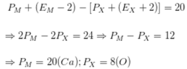
2(2PM+PX)+2NM+NX=140(1)
2(2PM+PX)=\(\dfrac{65,714}{100}.140=92\rightarrow\)2PM+PX=46(2)
-Thế (2) vào (1) ta được: 2NM+NX=48(3)
PM+NM-(PX+NX)=23(4)
-Từ (2,3) suy ra: 2(PM+NM)+PX+NX=94(5)
-Giải hệ (4,5) có được: PM+NM=39(M: K) và PX+NX=16(X:O)