Trong HC XHn có chứa 17.65% là H. Biết hợp chất này có tỷ khối so với khí Metan CH4 là 1,0625.X là nguyên tố nào ?![]() Các bạn gúp mình với
Các bạn gúp mình với
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

phân tử khối của XHn=1,0625.(12+4)=17
=> % MH=\(\frac{n.1}{17}.100=17,65\)
=> n\(\)=3
=> X=17-3=14=> X là Nito (N)

a/
Trong A có %0 = \(\frac{x16}{2R+x16}\)= \(\frac{22,22}{100}\)
<=> 1600x = 44,44R + 355,52 K
<-> 44,44R = 1244,48x
=> R=28x
=> x = 2 => R=56=> R là Fe
Trong B %0=\(\frac{y.16}{2R+16y}=\frac{30}{100}\)
<=> 1600y=60R+480y
<=> 60R=1120x
=> R=\(\frac{56}{3}x\)
=> y = 3 => R=56=> R là Fe
=> CTHH của A;B lần lượt là
Feo và Fe\(_2\)0\(_3\)

![]()
Ta có
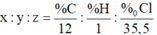
![]()
Do đó công thức phân tử của X có dạng(C2H4Cl)n
Mà ![]()
Vậy chất hữu cơ X là C4H8Cl2
Đáp án A.
tìm khối lượng mol của các chất khí sau so với CH4 có tỉ khối lần lượt là 2; 1,625 ; 0,125 và 1,0625

$M_{CH_4} = 16(đvC)$
Suy ra :
$M_1 = 16.2 = 32(đvC)$
$M_2 = 16.1,625 = 26(đvC)$
$M_3 = 16.0,125 = 2(đvC)$
$M_4 = 16.1,0625 = 17(đvC)$

câu 1
gọi CT NxHy
ta có
x: y = \(\frac{82,35}{14}:\frac{17,65}{1}\) = 1: 3
=> NH3

Mhc=1,0625.16=17
%H=\(\dfrac{M_H.100}{M_{hc}}=\dfrac{n.1.100}{17}=17,65\rightarrow n\approx3\)
X+3=17\(\rightarrow\)X=14(Nitơ: N)
lấy j chia j để sấp sỉ = 3