Hòa tan hoàn toàn m gam hỗn hợp X gồm Zn và ZnO vào 100gam dung dịch HCl 18,25%, sau phản ứng thu được 3,36 lit khí (đktc) và dung dịch Y có chứa 27,2 gam muối
a. Viết phương trình phản ứng và tính m
b. Tính C% chất tan trong dung dịch Y
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Y gồm NO (4x mol) và H2 (x mol)
Bảo toàn N => nNH4+ = 0,19 - 4x
Bảo toàn electron: 2nZn = 3nNO + 2nH2 + 8nNH4+
=> nZn = 0,76 - 9x
=> nZnO = 0,57 - 6,75x
nH+ = 1,62 = 4.4x + 2x + 10(0,19 - 4x) + 2(0,57 - 6,75x)
=> x = 0,04
Muối gồm Zn2+ (0,7), NH4+ (0,03), Na+ (0,19) và Cl-(1,62)
=> m muối = 107,92

Hỗn hợp Z chắc chắn có NO. MZ = 24,4 ⇒ Có H2.
⇒ Sơ đồ đường chéo ⇒ nNO : nH2 = 4 : 1
+ Đặt nNH4 = c ta có sơ đồ:
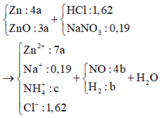
+ Phương trình bảo toàn điện tích: 4nZn = 8nNH4+ + 3nNO + 2nH2
8a = 8c + 4b×3 + b×2 8a – 14b – 8c = 0 (1).
+ Phương trình bảo toàn điện tích: 2nZn2+ + nNa+ + nNH4+ = nCl–
14a + 0,19 + c = 1,62 14a + c = 1,43 (2).
+ Phương trình bảo toàn nitơ: nNH4+ + nNOub> = nNaNO3
c×1 + 4b×1 = 0,19 4b + c = 0,19 (3)
+ Giải hệ (1) (2) và (3) ⇒ a = 0,1 và c = 0,03
⇒ mMuối = 7×0,1×65 + 0,19×23 + 0,03×18 + 1,62×35,5 = 107,92 gam
Đáp án D

Đáp án B
nOH- = 2nH2 = 0,4
nCl- = 2nH2 = 0,3
m↓ = 5,2 + 0,3.17 = 10,3 g
mmuối = 5,2+0,3.35,5= 15,85 g

n H2=\(\dfrac{1,12}{22,4}\)=0,05 mol
Zn+2HCl->ZnCl2+H2
0,05---0,1-----0,05---------0,05 mol
ZnO+2HCl->ZnCl2+H2
0,07----0,14---0,07
=m Zn=0,05.65=3,25g
m ZnCl2=0,05.136=6,8g
=>m ZnCl2 pt2 =16,32-6,8=9,52g
=>n ZnCl2=\(\dfrac{9,52}{136}\)=0,07 mol
=>m =3,25+0,07.81=8,92g
=>VHCl=\(\dfrac{0,24}{0,5}\)=0,48l=480ml

Đáp án B
Các phản ứng tạo kết tủa:
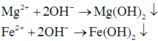
Dung dich X có ![]()
Dung dịch Y có ![]()
Mà ![]() nên OH-dư và
nên OH-dư và ![]()
Vậy ![]()
\(n_{HCl}=\dfrac{100.18,25}{36,5.100}=0,5mol\)
\(n_{H_2}=0,15mol\)
Zn+2HCl\(\rightarrow\)ZnCl2+H2(1)
ZnO+2HCl\(\rightarrow\)ZnCl2+H2O(2)
\(n_{ZnCl_2}=\dfrac{27,2}{136}=0,2mol\)
- Theo PTHH (1): \(n_{Zn}=n_{ZnCl_2\left(1\right)}=n_{H_2}=0,15mol\)
- Theo PTHH (2):\(n_{ZnO}=n_{ZnCl_2\left(2\right)}=0,2-0,15=0,05mol\)
- Theo PTHH (1,2): \(n_{HCl\left(pu\right)}=2n_{ZnCl_2}=2.0,2=0,4mol\)
\(n_{HCl\left(dư\right)}=0,5-0,4=0,1mol\)
m=\(m_{Zn}+m_{ZnO}=0,15.65+0,05.81=13,8g\)
\(m_{dd}=13,8+100-0,15.2=113,5g\)
\(C\%_{HCl}=\dfrac{0,1.36,5.100}{113,5}\approx3,22\%\)
\(C\%_{ZnCl_2}=\dfrac{27,2.100}{113,5}\approx24\%\)