cho 160ml dung dịch NaOH 0,2 M vào 100ml dung dịch Al2(SO4)3 0,5M. Tính khối lượng kết tủa thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
• 0,01 mol Al2(SO4)3 + V ml NaOH → ↓
Nung ↓ → 0,005 mol Al2O3
→ nAl(OH)3 = 0,005 × 2 = 0,01 mol.
• TH1: NaOH thiếu
AlCl3 + 3NaOH → Al(OH)3↓ + 3NaCl
nNaOH = 3 × nAl(OH)3 = 3 × 0,01 = 0,03 mol → VNaOH = 0,03 : 0,1 = 0,3 lít = 300ml.
• TH2: NaOH dư
Al2(SO4)3 + 6NaOH → 2Al(OH)3↓ + 3Na2SO4(*)
Al(OH)3 + NaOH → NaAlO2 + 2H2O (**)
Theo (*) nNaOH = 0,01 × 6 = 0,06 mol; nAl(OH)3 = 0,02 mol.
Theo (**) nAl(OH)3 phản ứng = 0,02 - 0,01 = 0,01 mol
→ nNaOH = 0,01 mol
→ ∑nNaOH = 0,06 + 0,01 = 0,07 mol
→ VNaOH = 0,07 : 0,1 = 0,7 = 700 ml

Đáp án : A
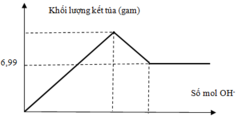
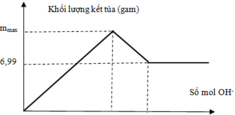
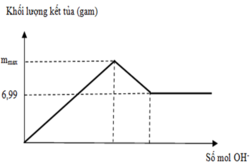
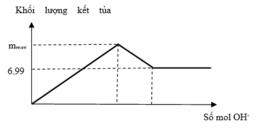
Khi đường thẳng nàm ngang thì lúc này kết tủa ổn địch chỉ còn duy nhất BaSO4
=> nBaSO4 = nSO4 = 0,3x = 0,03 mol => x = 0,1M
Nếu nBa(OH)2 = 0,02 ; nNaOH = 0,03 mol
=> nOH = 0,07 ; nAl3+ = 0,02
=> nAl(OH)3 = 4nAl3+ - nOH = 0,01 mol và nBaSO4 = nBa2+ = 0,02 mol
=> mkết tủa = 5,44g

\(n_{NaOH}=0,4mol\)
\(n_{Fe_2\left(SO_4\right)_3}=0,16.0,125=0,02mol\)
\(n_{Al_2\left(SO_4\right)_3}=0,16.0,25=0,04mol\)
Fe2(SO4)3+6NaOH\(\rightarrow\)2Fe(OH)3+3Na2SO4
0,02
Al2(SO4)3+6NaOH\(\rightarrow\)2Al(OH)3+3Na2SO4
0,04
Số mol NaOH(Pu)=6(0,02+0,04)=0,36mol
Số mol NaOH(dư)=0,4-0,36=0,04mol
Số mol Al(OH)3=0,04.2=0,08mol
Al(OH)3+NaOH\(\rightarrow\)NaAlO2+2H2O
Dựa vào tỉ lệ mol ta thấy Al(OH)3 còn dư=0,08-0,04=0,04mol
2Al(OH)3\(\rightarrow\)Al2O3+3H2O
Số mol Al2O3=0,04:2=0,02mol
2Fe(OH)3\(\rightarrow\)Fe2O3+3H2O
Số mol Fe2O3=0,02mol
mChất rắn=0,02(102+160)=5,24g
phương trình của NaOH và Al2(SO4)3 theo mình là sai
8NaOH + Al2(SO4)3  2NaAlO2 + 3Na2SO4 + 4H2O
2NaAlO2 + 3Na2SO4 + 4H2O



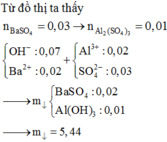
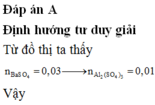


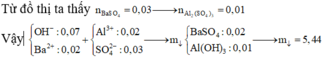
nNaOH = 0,032 (mol) => nOH- = 0,032 (mol)
nAl2(SO4)3 = 0,05 (mol) => nAl3+ = 0,1 (mol)
\(Al^{3+}+3OH^-\left(0,032\right)\rightarrow Al\left(OH\right)_3\downarrow\left(\dfrac{0,032}{3}\right)\)
=> m kết tủa = 0,832 (g)