Cho một lượng CaCO3 tác dụng hoàn toàn với dd HCl 32,85%. Sau phản ứng thu được dd X trong đó nồng độ phần trăm của dd HCl là 24,195%. Thêm vào dd X một lượng bột MgCO3 khuấy đều cho phản ứng xảy ra hoàn toàn thu được dd Y trong đó nồng độ HCl còn lại là 21,11%. Tính nồng độ % các muối trong dd Y.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Chọn 1 mol HCl ban đầu. Gọi n C a C O 3 = x
Có phản ứng: C a C O 3 + 2 H C l → C a C l 2 + C O 2 + H 2 O (1)
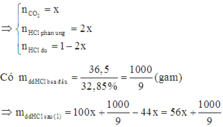
Do đó nồng độ phần trăm của HCl sau phản ứng (1) là:
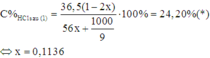
Do đó sau phản ứng (1) dung dịch X có mx = 117,47; nHCl dư = 0,7728
Gọi n M g C O 3 = y . Có phản ứng:
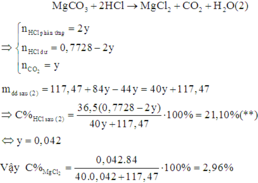
Do trong quá trình tính toán, ta có nhiều bước làm tròn nên dẫn đến sai số.
Khi đó ta sẽ chọn đáp án gần với kết quả tính được nhất.

Đáp án D
Giả sử có 100 gam dung dịch HCl 32,85% thì khối lượng HCl là 32,85 gam.
nHCl= 32 , 85 36 , 5 = 0,90 mol
- Gọi số mol của CaCO3 là x (mol). Phản ứng:
CaCO3 + 2HCl → CaCl2 + H2O + CO2 (1)
x 2x x x
Từ (1) và đề ra: nHCldư = (0,90 - 2x) mol
Khối lượng dung dịch X sau phản ứng (1): 100 + 100x – 44x = (100 + 56x) gam
Theo đề ra: C%HCl = ( 0 , 90 - 2 x ) . 36 , 5 100 + 56 x . 100 % = 24,195% => x = 0,1 mol
Vậy sau p/ư (1) nHCl còn lại = 0,7mol
- Cho MgCO3 vào dung dịch X, có p/ư:
MgCO3 + 2HCl → MgCl2 + H2O + CO2 (2)
y 2y y y
Sau p/ư (2) nHCl dư = 0,7-2y
Khối lượng dung dịch Y là: (105,6 + 84y - 44y) gam hay (105,6 + 40y) gam
Từ (2) và đề ra: C%HCl trong Y = ( 0 , 7 - 2 y ) . 36 , 5 105 , 6 + 40 y . 100% = 21,11% => y = 0,04 mol
Dung dịch Y chứa 2 muối CaCl2, MgCl2 và HCl dư:
C%(CaCl2) = 0 , 1 . 111 107 , 2 . 100 % = 10 , 35 %
C%(MgCl2) = 0 , 04 . 95 107 , 2 . 100 % = 3 , 54 %

=> n HCl = 0,9 mol
lúc sau , dễ thấy chỉ có Ca2+Ca2+ và 1 O trong CaCO3CaCO3 ở lại dd
gọi nCaCO3=anCaCO3=a
ta có pt
36,5 (0,9 - 2a) = 0,242 (100 + 56a)
\Leftrightarrow a = 0,0999 = 0,1 mol
số HCl còn lại trong dd X là 0,9 - 2 . 0,1 = 0,7 mol
tương tự với nMgCO3=bnMgCO3=b , dễ thấy
36,5 (0,7 - 2b) = 0,211 ( 100 + 56. 0,1 + 40b)
=> b = 0,0032956 = 0,0033 mol
từ a => mCaCL2=0,1.111=11,1gammCaCL2=0,1.111=11,1gam
b => mMgCl2=0,0033.95=0,3135gammMgCl2=0,0033.95=0,3135gam
m dd sau = 100 + 56 . 0,1 + 40 . 0,0033 = 105,732 gam
=> C % từng chất
CaCl2 : 10,5 %
MgCl2 = 0,297 %

Giả sử ban đầu có 100g dd HCl
\(\Rightarrow m_{HCl}=32,85\left(g\right)\)
\(\Rightarrow n_{HCl}=0,9\left(mol\right)\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
a___________2a_______a______a____________
\(m_{Dd_{Spu}}=100a+100-44a=56a+100\left(g\right)\)
\(n_{HCl_{Du}}=0,9-2a\left(mol\right)\)
\(m_{HCl_{du}}=32,85-73a\left(g\right)\)
\(\Rightarrow\frac{32,85-73a}{56a+100}=0,242\Leftrightarrow-73a+32,85=13,552a+24,2\)
\(\Rightarrow a=0,1\)
X có 0,1mol CaCl2 , 0,7mol HCl
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
b_________2b________b______b____________
\(m_{dd_{spu}}=84b+56.0,1+100-44b\)
\(=40b+105,6\left(g\right)\)
\(n_{HCl_{du}}=0,7-2b\left(mol\right)\)
\(\Rightarrow m_{HCl_{du}}=25,55-73b\)
\(\Rightarrow\frac{25,55-73b}{40b+105,6}=0,2111\)
\(\Leftrightarrow25,55b-73b=8,444b+22,29216\)
\(\Leftrightarrow b=0,04\)
\(\Rightarrow\) Y có 0,1mol CaCl2 , 0,04mol MgCl2 và HCl dư
\(\Rightarrow C\%_{CaCl2}=\frac{0,1.111.100}{40.0,04+105,6}=10,35\%\)
\(\Rightarrow C\%_{MgCl2}=\frac{0,04.95.100}{40.0,04+105,6}=3,54\%\)

a) \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2HCl + CaCO3 → CaCl2 + CO2 + H2O
Mol: 0,4 0,2 0,2
b) \(C\%_{ddHCl}=\dfrac{0,4.36,5.100\%}{100}=14,6\%\)
c) \(m_{CaCl_2}=0,2.101=20,2\left(g\right)\)
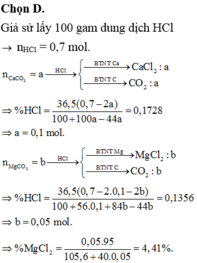
=> n HCl = 0,9 mol
lúc sau , dễ thấy chỉ có Ca2+Ca2+ và 1 O trong CaCO3CaCO3 ở lại dd
gọi nCaCO3=anCaCO3=a
ta có pt
36,5 (0,9 - 2a) = 0,242 (100 + 56a)
\Leftrightarrow a = 0,0999 = 0,1 mol
số HCl còn lại trong dd X là 0,9 - 2 . 0,1 = 0,7 mol
tương tự với nMgCO3=bnMgCO3=b , dễ thấy
36,5 (0,7 - 2b) = 0,211 ( 100 + 56. 0,1 + 40b)
=> b = 0,0032956 = 0,0033 mol
từ a => mCaCL2=0,1.111=11,1gammCaCL2=0,1.111=11,1gam
b => mMgCl2=0,0033.95=0,3135gammMgCl2=0,0033.95=0,3135gam
m dd sau = 100 + 56 . 0,1 + 40 . 0,0033 = 105,732 gam
=> C % từng chất
CaCl2 : 10,5 %
MgCl2 = 0,297 %