hòa tan 1 4g một kim loại kiềm vào nước. Để trung hòa dung dịch thu được cần dùng 100ml dung dịch HCL 2M. Xác định kim loại kiềm đã dùng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{HCl}=0,1.1=0,1\left(mol\right)\)
PTHH: \(2A+2xH_2O\rightarrow2A\left(OH\right)_x+xH_2\)
\(2A\left(OH\right)_x+2xHCl\rightarrow2ACl_x+2xH_2O\)
=> \(n_A=\dfrac{0,1}{x}\left(mol\right)\Rightarrow M_A=\dfrac{2,3}{\dfrac{0,1}{x}}=23x\left(g/mol\right)\)
Xét x = 1 => MA = 23(Na)

Chọn đáp án A
Phản ứng trung hòa: H+ + OH– → H2O
||⇒ nOH– = nH+ = 25 × 3,65% ÷ 36,5 = 0,025 mol.
⇒ MX = 0,575 ÷ 0,025 = 23 ⇒ X là Natri (Na).

Giải thích:
nHCl = (25. 3,65%)/( 100%. 36,5) = 0,025 (mol) => ne = 0,025.2 = 0,05 (mol)
MX = 0,575 : 0,05 = 23 => Na
Đáp án A

Đề thiếu m
NaOH + HCl = NaCl + H2O
0,3 - - - - 0,3
=>số mol HCl pư là 0,1 mol
=>số mol OH- = số mol H+ = số mol HCl = 0,1 mol
=>số mol kiềm thổ là 0,05 mol
=>R = 6,85 / 0,05 = 137 => Ba
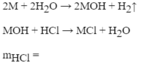
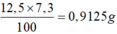

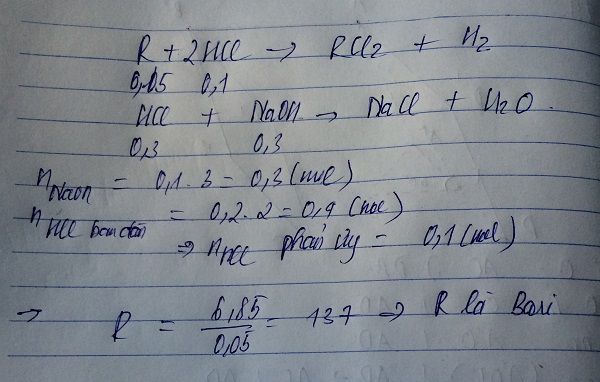

nHCl=0,2 mol
2R+2H2O\(\rightarrow\)2ROH+H2
ROH+HCl\(\rightarrow\)RCl2+H2O
\(n_R=n_{ROH}=n_{HCl}=0,2mol\)
R=\(\dfrac{m}{n}=\dfrac{1,4}{0,2}=7\left(Liti:Li\right)\)