cho 2,4g 1 oxit kim loại hóa trị II vào 10g dd HCl 21%. tìm KL của oxit
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi CTHH của oxit kim loại là RO
\(m_{HCl}=\dfrac{10.21,9\%}{100\%}=2,19\left(g\right)\\ n_{HCl}=\dfrac{2,19}{36,5}=0,06\left(mol\right)\\ RO+2HCl\xrightarrow[]{}RCl_2+H_2O\\ n_{RO}=\dfrac{0,06}{2}=0,03\left(mol\right)\\ M_{RO}=\dfrac{2,4}{0,03}=80\left(g/mol\right)\\ M_R=80-16=64\left(g/mol\right)\\ \Rightarrow R.là.đồng,Cu\)

Gọi kim loại hóa trị II là A
AO + 2HCl => ACl2 + H2O
mHCl = 10x21.9/100 = 2.19 (g)
==> nHCl = m/M = 2.19/36.5 = 0.06 (mol)
Theo pt ==> nAO = 0.03 (mol)
Ta có: A + 16 = m/n = 2.4/0.03 = 80
==> A = 80-16 = 64 (Cu)

hòa tan 9,4g M2O vào H2O được dd A có tính kiềm. chia thành 2 phần = nhau
- cho p1 vào 95ml dd HCl 1M thu đc dd làm xanh quỳ tím
- p2 cho vào 105ml dd HCl 1M thu được dd làm đỏ quỳ tím
xác định ct của oxit ban đầu

m(HCl)= 10*21.9/100= 2.19g
=> n(HCl)= 2.19/36.5=0.06 mol
Gọi kim loại đó là R ta có
RO + 2HCl => R(Cl)2 + H2O
0.03 <-- 0.06mol
=> M(RO)= 2.4/0.03= 80=> R= 80-16= 64
=> R là Cu

Bài 7:
Ta có: \(n_{ZnO}=\dfrac{16,2}{81}=0,2\left(mol\right)\)
\(m_{H_2SO_4}=100.40\%=40\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{40}{98}=\dfrac{20}{49}\left(mol\right)\)
PT: \(ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{\dfrac{20}{49}}{1}\), ta được H2SO4 dư.
Theo PT: \(n_{ZnSO_4}=n_{H_2SO_4\left(pư\right)}=n_{ZnO}=0,2\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=\dfrac{20}{49}-0,2=\dfrac{51}{245}\left(mol\right)\)
Ta có: m dd sau pư = 16,2 + 100 = 116,2 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{ZnSO_4}=\dfrac{0,2.161}{116,2}.100\%\approx27,71\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{\dfrac{51}{245}.98}{116,2}.100\%\approx17,56\%\end{matrix}\right.\)
Bài 8:
Gọi oxit cần tìm là AO.
Ta có: \(m_{HCl}=10.21,9\%=2,19\left(g\right)\Rightarrow n_{HCl}=\dfrac{2,19}{36,5}=0,06\left(mol\right)\)
PT: \(AO+2HCl\rightarrow ACl_2+H_2O\)
Theo PT: \(n_{AO}=\dfrac{1}{2}n_{HCl}=0,03\left(mol\right)\)
\(\Rightarrow M_{AO}=\dfrac{2,4}{0,03}=80\left(g/mol\right)\)
\(\Rightarrow M_A+16=80\Rightarrow M_A=64\left(g/mol\right)\)
→ A là Cu.
Vậy: Đó là oxit của đồng.
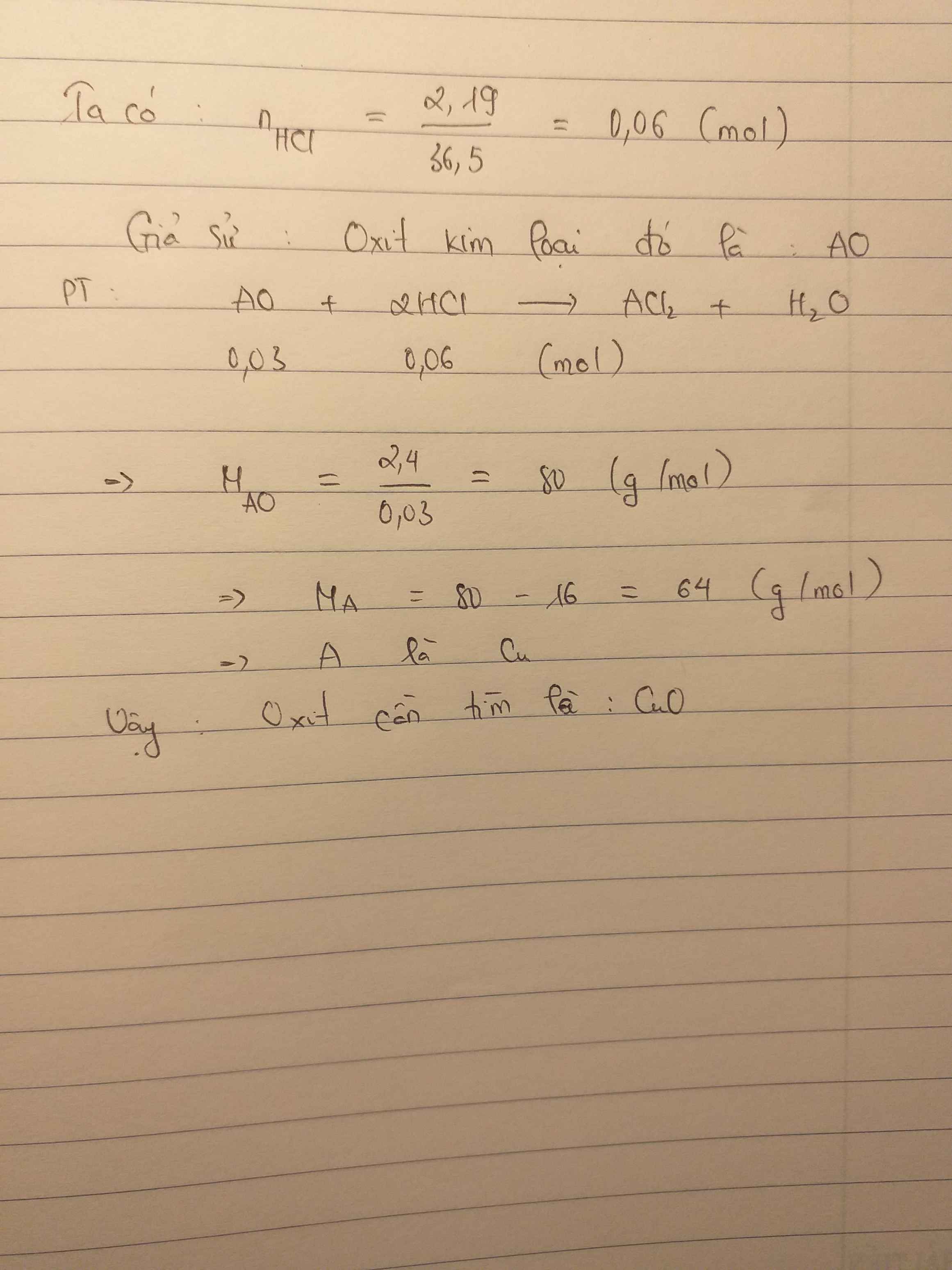
coi lại đề đi bạn
\(n_{HCl}=\dfrac{10.21\%}{36,5}=0,06\left(mol\right)\)
Gọi cthc: AO
\(AO+2HCl\rightarrow ACl_2+H_2O\)
A +16.....2
2,4.....0,06
=> A = 64
A là Cu
cthc: CuO