Trộn dung dịch chứa a (mol) AlCl3 với dung dịch chứa b (mol) NaOH.
Tính tỉ lệ a:b để thu được kết tủa.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
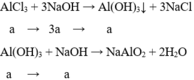
Nếu n NaOH = 4a thì kết tủa sẽ tan hết => để có kết tủa thì: n NaOH < 4a => b < 4a
=> a : b > 1 : 4

Gọi \(\left\{{}\begin{matrix}C_{M\left(A\right)}=aM\\C_{M\left(B\right)}=bM\end{matrix}\right.\)
Giả sử trộn 50ml dd A với 50ml dd B để thu được 100ml dd C
=> \(\left\{{}\begin{matrix}n_{NaOH}=0,05a\left(mol\right)\\n_{Ba\left(OH\right)_2}=0,05b\left(mol\right)\end{matrix}\right.\)
\(n_{BaSO_4}=\dfrac{9,32}{233}=0,04\left(mol\right)\)
nH2SO4 = 0,035.2 = 0,07 (mol)
PTHH: Ba(OH)2 + H2SO4 --> BaSO4 + 2H2O
0,04<----0,04<-------0,04
2NaOH + H2SO4 --> Na2SO4 + 2H2O
0,06<----0,03
=> \(\left\{{}\begin{matrix}0,05a=0,06\\0,05b=0,04\end{matrix}\right.\)
=> a = 1,2; b = 0,8
20 ml dd A chứa nNaOH = 0,02.1,2 = 0,024 (mol)
\(n_{Al_2O_3}=\dfrac{20,4}{102}=0,2\left(mol\right)\)
PTHH: 2NaOH + Al2O3 --> 2NaAlO2 + H2O
0,024-->0,012
Ba(OH)2 + Al2O3 --> Ba(AlO2)2 + H2O
0,188<---0,188
=> \(V_{dd.B}=\dfrac{0,188}{0,8}=0,235\left(l\right)=235\left(ml\right)\)

Chọn đáp án A
Xét phần 2: nBaSO4 = 0,24 mol ⇒ y = 0,24 ÷ 3 = 0,08 mol.
Xét phần 1: nOH– = 0,9 mol > 3nAl(OH)3 = 3 × 0,22
⇒ nOH– = 4nAl3+ - n↓ ⇒ nAl3+ = (0,22 + 0,9)/4 = 0,28 mol.
⇒ x = 0,28 - 0,08 × 2 = 0,12 ⇒ x : y = 3 : 2 ⇒ chọn A.
AlCl3: a mol
NaOH: b mol
Al3+a+→3OH−3a→Al(OH)3↓aAl3++3OH−→Al(OH)3↓a→3aa (kết tủa cực đại)
Al(OH)3a+→OH−a→AlO2−+2H2OAl(OH)3+OH−→AlO2−+2H2Oa→a
Nếu nNaOH = 4a thì kết tủa sẽ tan hết ⇒ để có kết tủa thì:
nNaOH < 4a ⇒ b < 4a
⇒ a : b > 1 : 4
a:b = 3:1