cho 2,16g hỗn hợp gồm Na, Al, Fe vào nước dư thì thu được 0,448l khí H2(đktc) và chất rắn B chứa hai kim loại. Cho toàn bộ B tác dụng hết với 200 g dung dịch CuSO4 có nồng độ là 4,8% thì thu được 3,2g Cu và dung dịch C. Tách dung dịch C và cho tác dụng với lượng vừa đủ dung dịch NaOH để thu được kết tủa lớn nhất. Nung kết tủa trong không khí đến khối lượng không đổi tì thu được chất rắn D. Xác định khối lượng của từng kim loại trong hỗn hợp A? Tính khối lượng chất rắn D? Tính nồng độ phần trăm các chất trong dung dịch C?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Định hướng tư duy giải
Ta có:
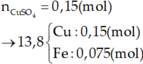
Dễ thấy 6 gam rắn là Fe2O3
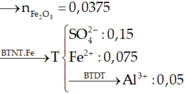
Có Al dư → Phần X phản ứng:
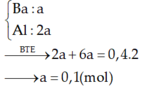
Chú ý: Vì chất tan thu được là Ba(AlO2)2→ tỷ lệ mol Ba : Al phải là 1 : 2
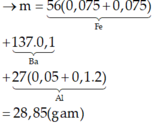

Chọn đáp án A
![]()
⇒ E gồm 3 kim loại thì đó là Ag, Cu và Fe dư ⇒ nFe dư = nH2 = 0,03 mol
Đặt n A g + = x mol; n C u 2 + = y mol ||→ mE = 8,12 gam = 108x + 64y + 0,03 × 56
![]()
![]()
Giải hệ có: x = 0,03 mol; y = 0,05 mol
![]()

PTHH: \(Al+NaOH+H_2O\rightarrow NaAlO_2+\dfrac{3}{2}H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
\(\Rightarrow n_{Al}=0,09\left(mol\right)\) \(\Rightarrow\%m_{Al}=\dfrac{0,04\cdot27}{2,6}\cdot100\%\approx41,54\%\)
Đặt \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow56a+64b=2,6-0,04\cdot27=1,52\) (1)
Mặt khác: \(n_{NO}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
Bảo toàn electron: \(3a+2b=0,075\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=n_{Fe}=0,022\left(mol\right)\\b=n_{Cu}=0,0045\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,022\cdot56}{2,6}\cdot100\%\approx47,38\%\\\%m_{Cu}\approx11,08\%\end{matrix}\right.\)
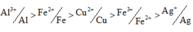
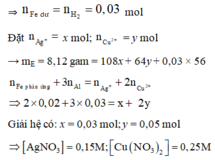
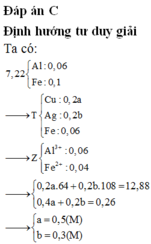


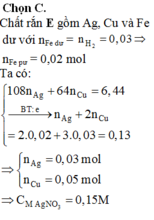

\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
- Số mol H2: \(n=\dfrac{V}{22,4}=\dfrac{0,448}{22,4}=0,02mol\)
- Chất rắn B chứa 2 kim loại là Fe và Al dư và theo PTHH 1 và 2 ta có số mol Al phản ứng 2= số mol NaOH=số mol Na
\(n_{CuSO_4}=\dfrac{200.4,8}{160.100}=0,06mol\)
2Al+3CuSO4\(\rightarrow\)Al2(SO4)3+3Cu
Fe+CuSO4\(\rightarrow\)FeSO4+Cu
\(n_{Cu}=\dfrac{3,2}{64}=0,05mol< n_{CuSO_4}=0,06mol\)
nên dung dịch C gồm Al2(SO4)3; FeSO4; CuSO4 dư 0,01 mol
- Tóm tắt: (Al2(SO4)3; FeSO4; CuSO4 )+NaOH\(\rightarrow\)(Al(OH)3; Fe(OH)2; Cu(OH)2)\(\overset{t^0}{\rightarrow}\) D(Al2O3; Fe2O3; CuO)
- Trong 2,16 gam hỗn hợp ta gọi số mol Na là x, Al phản ứng 2 là x và phản ứng 3 là a, Fe là z.
- Ta có: 23x+27(x+a)+56z=2,16 hay 50x+27a+56z=2,16
- Theo PTHH 1 và 2: \(n_{H_2}=\dfrac{1}{2}x+\dfrac{3}{2}x=0,02\) suy ra x=0,01
- Theo PTHH 3 và 4: \(n_{Cu}=\dfrac{3}{2}a+z=0,05\)
- Giải hệ:\(\left\{{}\begin{matrix}x=0,01\\50x+27a+56z=2,16\\\dfrac{3}{2}a+z=0,05\end{matrix}\right.\)
- Ta được: x=0,01; a=0,02; z=0,02
- Trong 2,16 g hỗn hợp có: Na 0,01 mol; Al 0,03 mol; Fe 0,02 mol)
- Vậy khối lượng từng kim loại trong A: Na=0,23g; Al=0,81g; Fe=1,12g
-Trong D có( Al2O3=\(\dfrac{1}{2}\)a=0,01 mol; Fe2O3 =\(\dfrac{1}{2}\)z=0,01mol; CuO=0,01mol)
\(m_D=0,01.102+0,01.160+0,01.80=3,42g\)
- Dung dịch C gồm Al2(SO4)3=0,01 mol; FeSO4= 0,02 mol; CuSO4 dư 0,01 mol
- Khối lượng dung dịch:
m=2,16+200-0,02.2-3,2=198,92g
\(\%m_{Al_2\left(SO_4\right)_3}=\dfrac{0,01.342.100}{198,92}\simeq1,72\%\)
\(\%m_{FeSO_4}=\dfrac{0,02.152.100}{198,92}\simeq1,53\%\)
\(\%m_{CuSO_4}=\dfrac{0,01.160.100}{198,92}\simeq0,8\%\)
tks bạn nha !! bạn học giỏi thật !! có gì chỉ mình thêm mấy bài tập Hóa nữa nha