Dùng khí hidro để khử hoàn toàn 6 gam một oxit sắt thì thu được 4,2 gam Fe.Tìm công thức phân tử của o xit sắt.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đặt công thức phân tử của oxit sắt là F e x O y (sắt có hóa trị 2x/y)
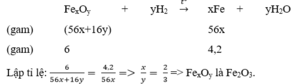

Gọi CT oxit sắt đó là FexOy.
PT: \(Fe_xO_y+yH_2\underrightarrow{t^o}xFe+yH_2O\)
Ta có: \(n_{Fe}=\dfrac{4,2}{56}=0,075\left(mol\right)\)
Theo PT: \(n_{Fe_xO_y}=\dfrac{1}{x}n_{Fe}=\dfrac{0,075}{x}\left(mol\right)\)
\(\Rightarrow M_{Fe_xO_y}=\dfrac{6}{\dfrac{0,075}{x}}=80x\left(g/mol\right)\)
\(\Rightarrow56x+16y=80x\Rightarrow24x=16y\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Vậy: Oxit sắt đó là Fe2O3.
Theo PT: \(n_{H_2}=\dfrac{y}{x}n_{Fe}=\dfrac{3}{2}.0,075=0,1125\left(mol\right)\Rightarrow V_{H_2}=0,1125.22,4=2,52\left(l\right)\)

\(n_{FeCl_2}=\dfrac{25.4}{127}=0.2\left(mol\right)\)
\(n_{H_2O}=\dfrac{5.4}{18}=0.3\left(mol\right)\)
\(Fe_xO_y+yH_2\underrightarrow{t^0}xFe+yH_2O\)
...........................\(x\) ..........\(y\)
...........................\(0.2\) ......\(0.3\)
\(\Rightarrow0.3x=0.2y\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{0.2}{0.3}=\dfrac{2}{3}\)
\(CT:Fe_2O_3\)
\(m_{Fe_2O_3}=0.2\cdot2\cdot160=64\left(g\right)\)

Đáp án : B
m H 2 S O 4 = 98g => mdd sau = 103,6g
=> n H 2 O t h ê m = 0,2 mol => nO(oxit) = 0,2 mol
Khi cho Fe + HCl : n H 2 = 0,15 mol = nFe
=> nFe : nO = 0,15 : 0,2 = 3 : 4
=> Fe3O4

\(n_{FeO}=\dfrac{3.2}{72}=\dfrac{2}{45}\left(mol\right)\)
\(FeO+H_2\underrightarrow{^{^{t^0}}}Fe+H_2O\)
\(\dfrac{2}{45}....\dfrac{2}{45}....\dfrac{2}{45}\)
\(V_{H_2}=\dfrac{2}{45}\cdot22.4=1\left(l\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{t^0}}FeCl_3\)
\(\dfrac{2}{45}.............\dfrac{2}{45}\)
\(m_{FeCl_3}=\dfrac{2}{45}\cdot162.5=7.22\left(g\right)\)

\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
Bảo toàn O: \(n_{O\left(oxit\right)}=n_{H_2O}=0,3\left(mol\right)\)
\(n_{FeCl_2}=\dfrac{25,4}{127}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,2 <-------------- 0,2
CTHH của oxit FexOy
=> x : y = 0,2 : 0,3 = 2 : 3
CTHH Fe2O3

a) Gọi CTHH của oxit sắt là $Fe_2O_n$
$Fe_2O_n + nCO \xrightarrow{t^o} 2Fe +nCO_2$
$n_{Fe} = \dfrac{22,4}{56} = 0,2(mol)$
$\Rightarrow n_{Fe_2O_n} = \dfrac{1}{2}n_{Fe} = 0,2(mol)$
$M_{oxit} = 56.2 + 16n = \dfrac{32}{0,2}=160$
Suy ra : n = 3
Vậy oxit cần tìm là $Fe_2O_3$
b) $n_{CO_2} = \dfrac{3}{2}n_{Fe} = 0,6(mol)$
$CO_2 +C a(OH)_2 \to CaCO_3 + H_2O$
$n_{CaCO_3} = n_{CO_2} = 0,6(mol)$
$m_{CaCO_3} = 0,6.100 = 60(gam)$
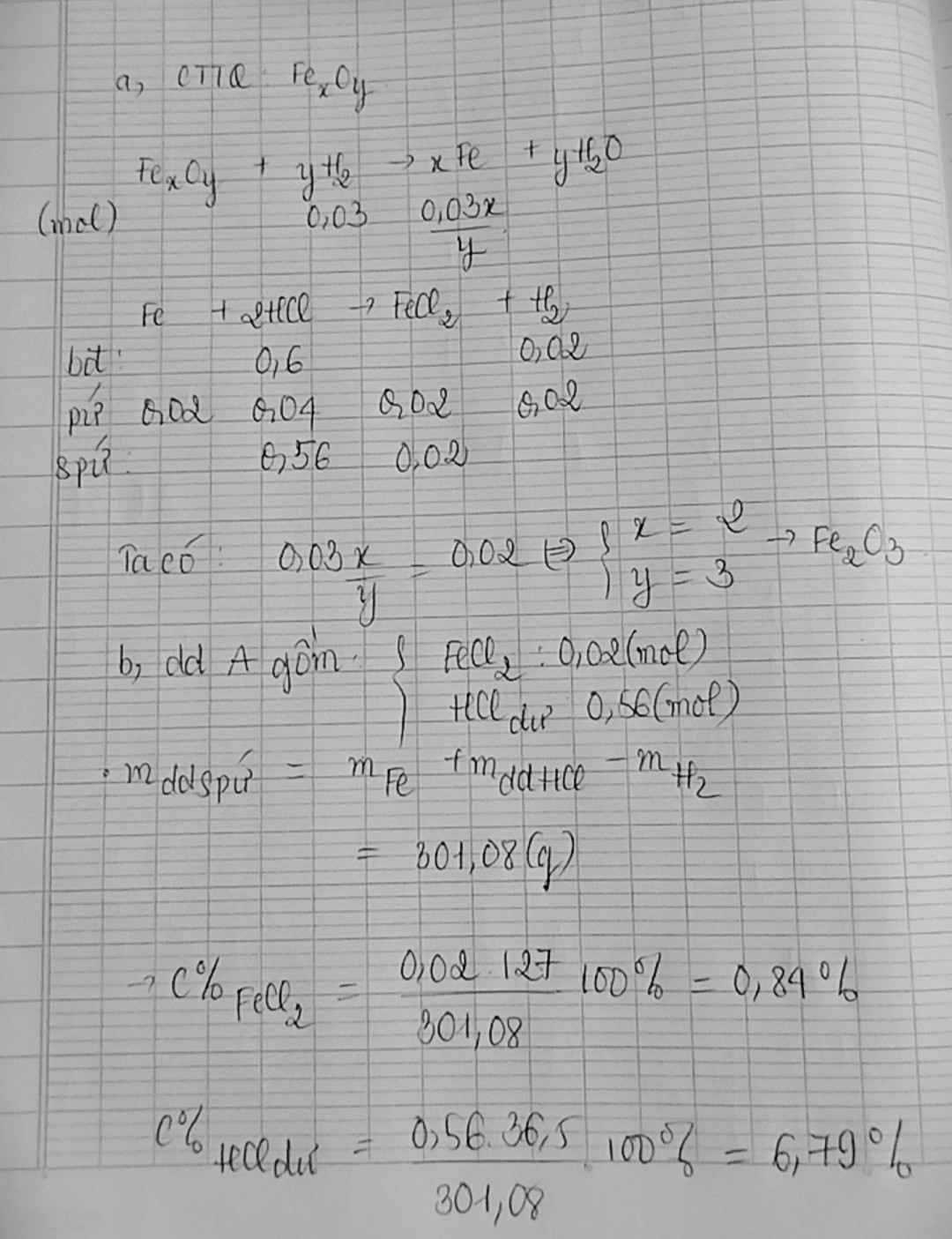
\(m_O=6-4.2=1.8\left(g\right)\)
\(n_{Fe}=\dfrac{4.2}{56}=0.075\left(mol\right)\)
\(n_O=\dfrac{1.8}{16}=0.1125\left(mol\right)\)
\(n_{Fe}:n_O=0.075:0.1125=2:3\)
\(CT:Fe_2O_3\)
Coi hỗn hợp oxit sắt gồm Fe và O
$n_{Fe} = \dfrac{4,2}{56} = 0,075(mol)$
$n_O = \dfrac{6 - 4,2}{16} = 0,1125(mol)$
Ta có :
$n_{Fe} : n_O = 0,075 : 0,01125 = 2 : 3$
Vậy oxit là $Fe_2O_3$