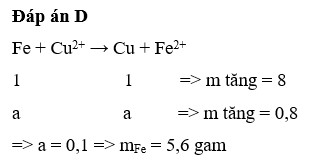cho một thanh sắt 60g vào dd CuSO4 .sau một thời gian thấy khối lượng của nó là 62g.Tính khối lượng CuSO4 phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đổi 200ml= 0,2l
Khối lượng đồng bám vào \(=203,2-200=3,2\left(g\right)\)
Đặt số mol của đồng là x
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
x_____ x______ x_________ x
Ta có : \(64x+56x=3,2\)
\(\rightarrow8x=3,2\rightarrow x=0,4\)
\(\rightarrow m=0,4.46=22,4\left(g\right)\)
\(\rightarrow CM_{CuSO4}=\frac{0,4}{0,2}=2M\)

Fe + CuSO4 = FeSO4 + Cu
Sau phản ứng khối lượng thanh sắt tăng lên, chứng tỏ có 1 lượng Cu bám lên thanh sắt.
Khối lượng Cu phản ứng là: 16,4 - 15,6 = 0,8 (g)
Số mol Cu là: 0,8 : 64 = 0,0125 (mol)
Theo PTHH: n Fe= nCu = 0,0125 (mol)
Khối lượng sắt tham gia phản ứng là: 0,0125 x 56 = 0,7(g)

Đáp án : D
Zn + Cu2+ -> Zn2+ + Cu
=> mgiảm = (65 – 64)x = 0,1g
=> x = 0,1 mol = nZn pứ
=> mZn pứ = 6,5g

Giải thích: Đáp án D
Zn + Cu2+ -> Zn2+ + Cu
=> mgiảm = (65 – 64)x = 0,1g
=> x = 0,1 mol = nZn pứ
=> mZn pứ = 6,5g

\(a.Fe+CuSO_4\rightarrow FeSO_4+Cu\\ b.Đặt:n_{Fe\left(pứ\right)}=x\left(mol\right)\\ m_{tăng}=m_{Cu\left(sinhra\right)}-m_{Fe\left(pứ\right)}=64x-56x=51-50\\ \Rightarrow x=0,125\left(mol\right)\\ m_{Cu}=0,125.64=8\left(g\right)\\ c.n_{FeSO_4}=n_{Fe\left(pứ\right)}=0,125\left(mol\right)\\ \Rightarrow m_{FeSO_4}=0,125.152=19\left(g\right)\)