1. Từ 320 tấn quặng pirit sắt FeS2 có chứa 45% lưu huỳnh đã sản xuất đc 405 tấn H2SO4. Hãy xác định hiệu suất của quá trình
2. Từ 1 tấn quặng pirit sắt chứa 80% FeS2.Có thể điều chế đc bnhiêu tấn dd H2SO4 60%. Biết rằng hiệu suất PỨ là 95%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A.
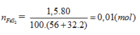
FeS2 → 2H2SO4 (Bảo toàn S)
0,01 → 0,02 (mol)
Do hiệu suất là 80%
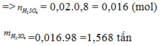

\(m_{FeS_2}=0.6\left(tấn\right)=0.6\cdot10^3\left(kg\right)\)
\(n_{FeS_2}=\dfrac{0.6\cdot10^3}{120}=\dfrac{10^3}{200}\left(kmol\right)\)
Dựa vào sơ đồ phản ứng :
\(n_{H_2SO_4}=2n_{FeS_2}=2\cdot\dfrac{10^3}{200}=\dfrac{10^3}{100}=10\left(kmol\right)\)
\(m_{H_2SO_4\left(tt\right)}=10\cdot\dfrac{98}{80\%}=1225\left(kg\right)\)
\(m_{dd_{H_2SO_4}}=\dfrac{1225}{98\%}=1250\left(kg\right)=12.5\left(tấn\right)\)
\(m_{FeS_2}=\dfrac{1.60}{100}=0,6\left(tấn\right)\)
=> \(m_{FeS_2\left(pư\right)}=\dfrac{0,6.80}{100}=0,48\left(tấn\right)\)
Cứ 1 mol FeS2 điều chế được 2 mol H2SO4
=> 120g FeS2 điều chế được 196g H2SO4
=> 0,48 tấn FeS2 điều chế được 0,784 tấn H2SO4
=> \(m_{ddH_2SO_4}=\dfrac{0,784.100}{98}=0,8\left(tấn\right)\)

ôi t làm nhầm....kq là
3,8 tấn ( cân bằng thêm 2 vào h2so4 là okok)
FeS2 ==> H2SO4
120g 98g
2,85( vì 5% tạp chất) 2,3275 (tấn)
vì H=80% ====> m H2SO4=1,3965( tấn). nhưng có C% H2SO4= 98%
VẬY mdd H2S04 là 1,425 tấn

Đáp án C.
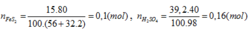
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%

\(PTHH:S+O_2\underrightarrow{t^o}SO_2\\ SO_2+\frac{1}{2}O_2\xrightarrow[V_2O_5]{t^o}SO_3\\ SO_3+H_2O\rightarrow H_2SO_4\)
\(m_{S\cdot trong\cdot FeS_2}=320.10^6.45\%=144.10^6\left(g\right)\)
\(n_S=\frac{144.10^6}{32}=45.10^5\left(mol\right)\)
Theo pt: \(n_S=n_{SO_2}=n_{SO_3}=n_{H_2SO_4}\)
\(\Rightarrow n_{H_2SO_4}=45.10^5\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=45.10^5.98=441.10^6\left(g\right)=441\left(ton\right)\)
\(H=\frac{441}{450}.100\%=98\left(\%\right)\)
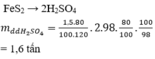

1) Bạn tự viết Các PTHH nhé
: Theo đề bài ta có :
\(mS\left(trong-qu\text{ặng}\right)=\dfrac{320.45}{100}=144\left(t\text{ấn}\right)\)
=> nS = \(\dfrac{144}{32}=4,5\left(mol\right)\)
Cách 1 : Ta có :
nH2SO4 = \(\dfrac{405}{98}\approx4,13\left(mol\right)\)
=> H = \(\dfrac{n\left(ch\text{ất}-thi\text{ếu}\right)}{n\left(ch\text{ất}-d\text{ư}\right)}.100\%=\dfrac{4,1}{4,5}.100\%\approx91,8\%\)
Cách 2 : Ta có : nS = nH2SO4 = 4,5 (mol) => mH2SO4 = 4,5 . 98 = 441 (g)
=> H = \(\dfrac{m\left(th\text{ực}-t\text{ế}-thu-\text{đ}\text{ư}\text{ợc}\right)}{m\left(t\text{ính}-theo-l\text{ý}-thuy\text{ết}\right)}.100\%=\dfrac{405}{441}.100\%\approx91,8\%\)
Vậy.............
ây za mình ghi nhầm ở trên chỗ tính r xin lỗi bạn nha