Nung X1 gam Cu với X2 gam O2 thì được chất rắn A1. Đun nóng A1 trong X3 gam H2SO4 98%. Sau khi hòa tan hết thu được dung dịch A2 và khí A3. Hấp thụ toàn bộ A3 bằng 200ml NaOH 0.15M tạo ra dung dịch chứa 2.3g muối. Khi cô cạn dung dịch A2 thu 30g tinh thể CuSO4.5H2O. Nếu cho A2 tác dụng dung dịch NaOH 1M thì để tạo ra chất kết tủa nhiều nhất phải dùng hết 300ml NaOH. Viết phương trình. Tính X1,X2,X3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nNaOH = 0,1.0,3 = 0,03 (mol)
Gọi \(\left\{{}\begin{matrix}n_{Na_2SO_3}=a\left(mol\right)\\n_{NaHSO_3}=b\left(mol\right)\end{matrix}\right.\)
=> 126a + 104b = 2,3
Bảo toàn Na: 2a + b = 0,03
=> a = 0,01 (mol); b = 0,01 (mol)
Bảo toàn S: \(n_{SO_2}=0,02\left(mol\right)\)
\(n_{CuSO_4}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
Bảo toàn Cu: nCu = 0,12 (mol)
=> a = 0,12.64 = 7,68 (g)
Bảo toàn S: \(n_{H_2SO_4}=n_{CuSO_4}+n_{SO_2}=0,12+0,02=0,14\left(mol\right)\)
=> \(m_{H_2SO_4}=0,14.98=13,72\left(g\right)\)
=> \(b=m_{dd.H_2SO_4}=\dfrac{13,72.100}{98}=14\left(g\right)\)
Bảo toàn H: \(n_{H_2O}=n_{H_2SO_4}=0,14\left(mol\right)\)
BTKL: \(m_{Cu}+m_{O_2}+m_{H_2SO_4}=m_{CuSO_4}+m_{SO_2}+m_{H_2O}\)
=> mO2 = 19,2 + 0,02.64 + 0,14.18 - 7,68 - 13,72 = 1,6 (g)
=> \(n_{O_2}=\dfrac{1,6}{32}=0,05\left(mol\right)\)
=> \(V_{O_2}=0,05.22,4=1,12\left(l\right)\)

Đáp án B
Vì H2SO4 đặc nóng dư nên khí A sinh ra là SO2.
Muối khan thu được là
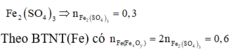
Vì dung dịch NaOH dư nên khỉ dẫn SO2 vào đung dịch NaOH chỉ xảy ra một phản ứng:
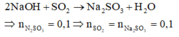
Coi oxit FexOy ban đầu là hỗn hợp của Fe và O.
Gọi nO = a.
Áp dụng định luật bảo toàn moi electron, ta có:


A 1 là CO, C O 2 ; A 2 là C O 2 ; A 3 là Cu, CuO dư; A 4 là C a C O 3 ; A 5 là C a H C O 3 2

⇒ Chọn A.
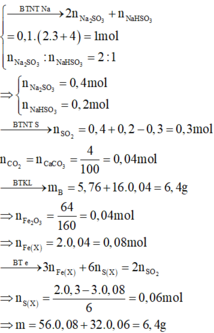




CÂU NÀO CÓ GOOGLE CÒN ĐĂNG LÀM GÌ
−2Cu+O2−to−>2CuO(1)
Do chất rắn sau pư td vớiH_2SO4H2SO4sinh ra khí nên A1 gồm CuO và Cu dư:
-CuO +H_2SO_4 -->CuSO_4 +H_2O (2)−CuO+H2SO4−−>CuSO4+H2O(2)
$-Cu(dư) +2H_2SO_4- ->CuSO_4 +SO_2 +2H_2O (3). $
Vậy A3 làSO_2SO2. Khi cho SO_2SO2 vào NaOH.Ta nhận thấy nNaOH=0,03mol. Mà nNaOH/2dd tạo thành là 2 muối:
-SO2 +NaOH ->NaHSO_3 (4)−SO2+NaOH−>NaHSO3(4)
-SO2 +2NaOH ->Na_2SO_3 +H_2O (5)−SO2+2NaOH−>Na2SO3+H2O(5)
-ta thấy:
trog 250g CuSO_4.5H_2OCuSO4.5H2Ocó 160g CuSO_4.
Vậy trog 30g -->x=160.30/250=19,2g =>n_{CuSO_4}nCuSO4=19,2/160=0,12mol.
Để tạo kết tủa nhiều nhất với A2 cần 0,3.1=0,3mol NaOH
=>nNaOH/2>n{CuSO_4} =>vậy A2 chứa dd CuSO_4CuSO4vàH_2SO_4H2SO4 dư:
-CuSO_4 +2NaOH ->Na_2SO_4 +Cu(OH)_2 (6)−CuSO4+2NaOH−>Na2SO4+Cu(OH)2(6)
-H_2SO_4 +2NaOH ->Na_2SO_4 +2H_2O (7)−H2SO4+2NaOH−>Na2SO4+2H2O(7)
gọi x,y là số mol của SO_2SO2 ở 4 và 5. Ta được:
x+2y=0,03 và 104x +126y =2,3 =>x=y =0,01mol.
Vậy: n_{SO_2}nSO2=0,01+0,01=0,02mol.
Theo 3: $n_{Cu dư}$= 0,02mol.
n_{H_2SO_4}nH2SO4(3)=2n_{SO_2}nSO2=2.0,02=0,04mol.
n_{CuSO_4(3)}nCuSO4(3)=n_{SO_2}nSO2=0,02mol=>n_{CuSO_4(2)}nCuSO4(2)=0,12...
Theo 2: n_{H_2SO_4(2)}nH2SO4(2) = n_{CuSO_4(2)}nCuSO4(2)=0,1mol.
n_{CuO}nCuO = n_{CuSO_4}nCuSO4(2) = 0,1mol.
Theo 1:n_{O_2}nO2 = nCuO/2 = 0,1/2 = 0,05mol
nCu=nCuO = 0,1mol.
=>X1=mCu = (0,1+0,02).64=7,68g.
X2=m_{O_2}mO2=0,05.32=1,6g.
-theo 6:
n{NaOH(6)} = 2n_{CuSO_4}nCuSO4 = 0,12.2=0,24mol =>n_{NaOH}nNaOH...
=>m_{H_2SO_4}mH2SO4 = (0,03+0,1+0,04).98=16,66g =>md...
Nguồn: Yahoo: