Cho 28,4 gam hỗn hợp 2 muối cacbonat của 2 kim loại hoá trị I tác dụng với dd HCl thu được 6,72 lít khí đktc .
A, Tính khối lượng muối clorua
B, Xác định 2 kim loại biết 2 kim loại ở 2 chu kì liên tiếp .
C, Khí trên được hấp thụ hoàn toàn trong 1,25 lít Ba(OH)2 thu được 39,4g kết tủa . Tính nồng độ Ba(OH)2 .

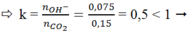
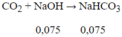

a,
\(28,4g\left\{{}\begin{matrix}X_2CO_3\\MgCO_3\end{matrix}\right.\)\(+HCl-->6,72l\)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(X_2CO_3+2HCl-->2XCl+H_2O+CO_2\)
\(Y_2CO_3+2HCl-->2YCl+H_2O+CO_2\)
Theo định luật bảo toàn khối lượng :
\(m_{M_2CO_3}+m_{HCl}=m_{muối}+m_{H_2O}+m_{CO_2}\)
\(28,4+21,9=m_{2.muối}+5,4+13,2\)
\(m_{2.muối}=31,7g\)
b,
\(M_X< M_{\overline{M}}< M_Y\)
Ta giải theo khối lượng mol trung bình :
\(M_2CO_3\left(0,3\right)+2HCl\left(0,6\right)-->2\overline{M}Cl\left(0,3\right)+H_2O\left(0,3\right)+CO_2\left(0,3\right)\)
\(m_{HCl}=0,6.36,5=21,9\left(g\right)\)
\(m_{CO_2}=0,3.44=13,2\left(g\right)\)
\(m_{H_2O}=0,3.18=5,4\left(g\right)\)
Theo định luật bảo toàn khối lượng :
\(m_{\overline{M_2}CO_3}=m_{\overline{M}Cl}+m_{H_2O}+m_{CO_2}-m_{HCl}\)
\(=31,7+5,4+13,2-21,9=38,4\left(g\right)\)
\(M_{\overline{M_2}CO_3}=\dfrac{m}{n}=\dfrac{28,4}{0,3}=94,67\left(g\right)\)
\(=>2M_{\overline{M}}+60=94,67\)
\(2M_{\overline{M}}=34,67\)
\(M_{\overline{M}}=17,335\left(g\right)\)
\(7\left(Li\right)< 17,335< 23\left(Na\right)\)
\(=>X:Li\)
\(Y:Na\)
\(c,CO_2\left(0,1\right)+Ba\left(OH\right)_2\left(0,05\right)-->Ba\left(HCO_3\right)_2\)
\(CO_2\left(0,2\right)+Ba\left(OH\right)_2\left(0,2\right)-->BaCO_3\downarrow\left(0,2\right)+H_2O\)
\(n_{BaCO_3}=\dfrac{39,4}{197}=0,2\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,2+0,05=0,25\left(mol\right)\)
\(C_{MBa\left(OH\right)_2}=\dfrac{0,25}{1,25}=2M\)