1. Cho 15.3 gam oxit của kim loại hóa trị II vào nước thu được 200gam dung dịch bazơ với nồng độ 8,55%. Hãy xác định công thức của oxit trên
2 Cho 38.4 gam một oxit axit của phi kim X có hóa trị IV tác dụng vừa đủ với dd NaOH thu được 400gam dd muối nồng độ 18,9%. Xác định công thức của oxit

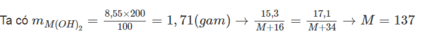

bài 1:
Gọi oxit kim loai cần tìm là M
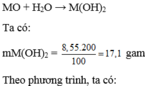
=> PTHH: MO + H2O ----> M(OH)2
m\(M\left(OH\right)_2\) = \(\dfrac{200.8,55\%}{100\%}=17,1\) (g)
=> n\(M\left(OH\right)_2\) = \(\dfrac{17,1}{M+34}\left(mol\right)\)
Theo PTHH: n\(MO\) = n\(M\left(OH\right)_2\) = \(\dfrac{17,1}{M+34}\left(mol\right)\)
=> m\(MO\) = \(\dfrac{17,1}{M+34}.\left(M+16\right)\)= \(\dfrac{17,1M+273,6}{M+34}=15,3\left(g\right)\)
=> 17,1M + 273,6 = 15,3M + 520,2
<=> 1,8M = 246,6
<=> M = 137
=> M là Ba
=> CTHH của oxit: BaO
2, CT: XO2
\(n_{Na_2XO_3}=\dfrac{18,9.400}{100}=75,6g\)
XO2 + 2NaOH\(\rightarrow\) Na2XO3 + H2O
pt: X + 32 46+ X +48 (g)
de: 38,4 75,6 (g)
Ta co: \(75,6\left(X+32\right)=38,4\left(94+X\right)\)
\(\Leftrightarrow75,6X+2419,2=38,4X+3609,6\)
\(\Leftrightarrow37,2X=1190,4\)
\(\Rightarrow X=32\left(đvC\right)\)\(\Rightarrow X\) là lưu huỳnh
CT: SO2