Cho hỗn hợp M gồm NaCl và NaBr. Lấy 12,59g hỗn hợp đó hòa tan hết vào nước, thu được dung dịch A. Cho lượng dư khí clo đi chậm qua A.Sau khi cô cạn cẩn thận dung dịch thì thu được 11,7g muối khan.Tính hàm lượng % theo khối lượng của muối trong hỗn hợp M
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(\left\{{}\begin{matrix}nNaCl=x\\nNaBr=y\\nNaI=z\end{matrix}\right.\)
ta có : \(58,5x+103y+150z=5,76\left(1\right)\)
TN1:
\(Br_2+2NaI\rightarrow2NaBr+I_2\)
z ----> z
\(\Rightarrow m_{muối}=mNaBr+mNaCl=103\left(y+z\right)+58,5x=5,29\left(2\right)\)
Từ (1) và (2) => z =0,01
TN2:
\(Cl_2+2NaI\rightarrow2NaCl+I_2\)
0,01 0,01
\(Cl_2+2NaBr\rightarrow2NaCl+I_2\)
\(nNaCl=nCl^-=0,05\rightarrow mNaCl=2,925\left(g\right)\)muối khan ngoài NaCl còn muối khác.Do \(I^-\) có tính khử mạnh hơn \(Br^-\) nên NaI sẽ hết trước và sau hai phản ứng NaBr còn dư.
\(nNaBr\left(dư\right)=t\)
\(\Rightarrow nNaCl=0,05=0,01+y-t+x\)
\(m_{muối}=mNacl+mNaBr\Rightarrow mNaBr_{\left(dư\right)}=3,955-0,05.58,5=1,03\)
\(\Rightarrow t=0,01\)
\(\Rightarrow x+y=0,05\left(3\right)\)
(1) ; (3) ; => \(x=0,02;y=0,03\)
\(\Rightarrow mNaCl=1,17\left(g\right)\)

NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%
NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%

Chọn đáp án C
Gọi số mol của NaBr là x mol; NaI là y mol.
Cho B r 2 vào dung dịch A, chỉ NaI phản ứng.
NaI + 1 2 Br2 → NaBr + 1 2 I2
1 mol NaI → 1 mol NaBr khối lượng giảm 47g
→ n N a I = 7 , 05 47 = 0,15 mol = y
Khi sục khí Clo vào dung dịch A, cả NaBr và NaI phản ứng.
m m u ố i g i ả m = x.(80 – 35,5) + y (127-35,5) = 22,625 g
→ x = 0,2 mol
ð % m N a B r = 0 , 2 . 103 0 , 2 . 103 + 0 , 15 . 150 .100(%) = 47,80(%)

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
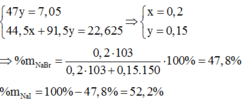

Đáp án B
Gọi x, y là số mol NaCl và NaI trong hh X
m(X) = m(NaCl) + m(NaI) = 58,5x + 150y = 104,25g (1)
Sục khí Cl2 dư vào dd A:
NaI + 1/2Cl2 → 1/2I2 + NaCl
y → y
mmuối = m(NaCl) = 58,5.(x+y) = 58,5g
→ x + y = 1mol (2)
Giải hệ PT (1), (2) ta được: x = 0,5mol và y = 0,5mol
mNaCl = 0.5.58,5 = 29,25 (g)

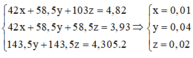
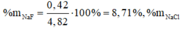
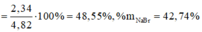
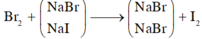
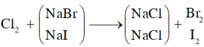
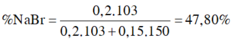
Gọi a, b lần lượt là số mol của NaCl, NaBr
\(\Rightarrow58,5a+103b=12,59\left(I\right)\)
\(2NaBr\left(b\right)+Cl_2\rightarrow2NaCl\left(b\right)+Br_2\)
Dung dịch muối khan là: \(\left\{{}\begin{matrix}NaCl:a\left(mol\right)\\NaCl:b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow58,5\left(a+b\right)=11,7\left(II\right)\)
Từ (I) và (II) \(\Rightarrow\left\{{}\begin{matrix}a=0,18\\b=0,02\end{matrix}\right.\)\(\left(mol\right)\)
Suy ra phần trăm khối lượng mỗi muối trong M