Cho 11g hỗn hợp gồm hai kim loại Fe và Al tác dụng với 400ml dd\(H_2SO_4\)1M. Tính khối lượng mỗi kim loại ban đầu và \(C_M\) của mỗi muối thu được. (\(V_{dd}\) thay đổi không đáng kể)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\left(1\right)\)
x x
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\left(2\right)\)
y 1,5y
Đổi: 400ml = 0,4l
\(n_{H_2SO_4}=C_M.V=1.0,4=0,4\left(mol\right)\)
Gọi x,y lần lượt là số mol của Fe, Al
Từ(1),(2) =>\(\left\{{}\begin{matrix}x+1,5y=0,4\\56x+27y=11\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(m_{Al}=0,2.27=5,4\left(g\right)\)
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
\(C_{M_{FeSO_4}}=\dfrac{0,1}{0,4}=0,25M\)
\(C_{M_{Al_2\left(so_4\right)_3}}=\dfrac{0,1}{0,4}=0,25M\)

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Ag}=y\left(mol\right)\end{matrix}\right.\Rightarrow27x+108y=4,2\left(1\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,1 0,05 0,15
\(\Rightarrow m_{Al}=0,1\cdot27=2,7g\)
\(\Rightarrow m_{Ag}=4,2-2,7=1,5g\)
a)\(\%m_{Al}=\dfrac{2,7}{4,2}\cdot100\%=64,28\%\)
\(\%m_{Ag}=100\%-64,28\%=35,72\%\)
b)\(m_{muối}=0,05\cdot342=17,1g\)

a) PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
b) Ta có: \(\Sigma n_{H_2}=\dfrac{3,024}{22,4}=0,135\left(mol\right)\)
Gọi số mol của Fe là \(a\) \(\Rightarrow n_{H_2\left(1\right)}=a\)
Gọi số mol của Al là \(b\) \(\Rightarrow n_{H_2\left(2\right)}=\dfrac{3}{2}b\)
Ta lập được hệ phương trình:
\(\left\{{}\begin{matrix}a+\dfrac{3}{2}b=0,135\\56b+27b=4,14\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,045\\b=0,06\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,045\cdot56=2,52\left(g\right)\\m_{Al}=1,62\left(g\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{2,52}{4,14}\cdot100\%\approx60,87\%\\\%m_{Al}=39,13\%\end{matrix}\right.\)
c) PTHH: \(FeCl_2+2NaOH\rightarrow2NaCl+Fe\left(OH\right)_2\downarrow\)
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\)
\(4Fe\left(OH\right)_2+O_2\underrightarrow{t^o}2Fe_2O_3+4H_2O\)
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
Theo các PTHH: \(\left\{{}\begin{matrix}n_{Fe\left(OH\right)_2}=n_{FeCl_2}=0,045mol\\n_{Al\left(OH\right)_3}=n_{AlCl_3}=0,06mol\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_2O_3}=0,0225mol\\n_{Al_2O_3}=0,03mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,0225\cdot160=3,6\left(g\right)\\m_{Al_2O_3}=0,03\cdot102=3,06\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{chấtrắn}=3,06+3,6=6,66\left(g\right)\)

a) Fe +2 HCl -> FeCl2 + H2
x____2x______x____x(mol)
2 Al + 6 HCl -> 2 AlCl3 + 3 H2
y____3y______y________1,5y(mol)
b) nH2= 0,05(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}56x+27y=1,66\\x+1,5y=0,05\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,02\end{matrix}\right.\)
=> mFe=0,02.56= 1,12(g)
mAl=0,02.27=0,54(g)

Đáp án D.
![]()
Giả sử AgNO3 phản ứng hết khi đó Ag+ chuyển hết thành Ag
nAg = = 0,4 mol à mAg = 0,4.108 = 43,2 gam > mA (=32,4 gam)
-> AgNO3 chưa phản ứng hết.
mA = mAg = 32,4 gam à nAg = 0,3 mol
Gọi số mol của Mg và Cu lần lượt là x và y mol
Theo bài ta có: 24x + 64y = 5,6 (1)
Ta có:
Mg à Mg+2 + 2e Ag + e à Ag+
x 2x 0,3 0,3
Cu à Cu+2 + 2e
y 2y
Bảo toàn e ta có: 2x + 2y = 0,3 (2)
Từ (1) và (2) ta có hệ phương trình:
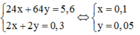
Khối lượng mỗi kim loại trong hỗn hợp đầu là:
mMg = 0,1.24 = 2,4 gam; mCu = 0,05.64 = 3,2 gam.

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
a)\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1 0,1
\(m_{Fe}=0,1\cdot56=5,6\left(g\right)\)
b)\(\Rightarrow\%m_{Fe}=\dfrac{5,6}{12}\cdot100\%=46,67\%\) \(\Rightarrow\%m_{Cu}=100\%-46,67\%=53,33\%\)
c)\(n_{NaOH}=0,1\cdot1=0,1mol\)
\(2NaOH+FeCl_2\rightarrow Fe\left(OH\right)_2+2NaCl\)
0,1 0,1 0,1
\(m_{Fe\left(OH\right)_2}=0,1\cdot90=9\left(g\right)\)
Đổi:400ml=0,4l
Gọi x;2y là số mol Fe,Al
Theo gt:\(m_{hhKL}\)=\(m_{Fe}+m_{Al}\)=56x+27y.2
=56x+54y=11(1)
Ta có PTHH:
Fe+\(H_2SO_4\)->\(FeSO_4\)+\(H_2\)(1)
x..........x................x.................(mol)
4Al+6\(H_2SO_4\)->2\(Al_2(SO_4)_3\)+3\(H_2\)(2)
2y...........3y...............y.........................(mol)
Ta có:\(C_{MddH_2SO_4}\)=1M
=>\(n_{H_2SO_4}\)=1.0,4=0,4mol
Theo PTHH(1);(2):
\(n_{H_2SO_4}\)=x+3y=0,4(2)
Từ (1);(2)=>\(\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)=>\(\left\{{}\begin{matrix}m_{Al}=54y=54.0,1=5,4\left(g\right)\\m_{Fe}=56x=56.0,1=5,6\left(g\right)\end{matrix}\right.\)
Theo PTHH(1);(2):\(n_{FeSO_4}\)=x=0,1(mol)
\(n_{Al_2\left(SO_4\right)_3}\)=y=0,1(mol)
Vậy \(C_{M\left(FeSO_4\right)}\)=0,1:0,4=0,25M
\(C_{MAl_2\left(SO_4\right)_3}\)=0,1:0,4=0,25M
\(n_{H_2SO_4}=0,4.1=0,4\left(mol\right)\)
Gọi x, y lần lượt là số mol của Al, Fe
Pt: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\) (1)
x \(\rightarrow\dfrac{3x}{2}\) \(\rightarrow0,1mol\)
Pt: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\) (2)
y \(\rightarrow y\) \(\rightarrow0,1mol\)
(1)(2) \(\Rightarrow\left\{{}\begin{matrix}1,5x+y=0,4\\27x+56y=11\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(m_{Al}=0,2.27=5,4\left(g\right)\)
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
\(C_{M_{Al_2\left(SO_4\right)_3}}=\dfrac{0,1}{0,4}=0,25M\)
\(C_{M_{FeSO_4}}=\dfrac{0,1}{0,4}=0,25M\)