Giải giúp mình bài này đi cho 13,5 g kim loại R chưa rõ hoá trị phản ứng với HCl vừa đủ, sau phản ứng thu được 16,8 lít Hiđrô đktc. Tìm tên kim loại R. Giúp mình nha mình đang cần gấp
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_R=\dfrac{75,6}{M_R}mol\)
\(n_{R_2O_n}=\dfrac{104,4}{2M_R+16n}mol\)
\(R_2O_n+H_2\rightarrow\left(t^o\right)2R+nH_2O\)
\(\dfrac{104,4}{2M_R+16n}\) -----> \(\dfrac{208,8}{2M_R+16n}\) ( mol )
\(\Rightarrow\dfrac{208,8}{2M_R+16n}=\dfrac{75,6}{M_R}\)
\(\Leftrightarrow208,8M_R=151,2M_R+1209,6n\)
\(\Leftrightarrow57,6M_R=1209,6n\)
\(\Leftrightarrow M_R=21n\)
Xét :
n=1 => Loại
n=2 => Loại
n=3 => Loại
\(n=\dfrac{8}{3}\) => R là sắt ( Fe )
Vậy Kim loại đó là sắt ( Fe )
\(\Rightarrow n_{H_2}=\dfrac{75,6}{2.56}=0,675mol\)
\(V_{H_2}=0,675.22,4=15,12l\)

Gọi X là kim loại đem ra phản ứng
nH2 = 0,3136/22,4 = 0,014 mol
PTHH: 2X + 2xHCl -> 2XClx + xH2
2mol 2x mol 2 mol x mol
0,028/x <-- 0,028 mol <-- 0,014 mol
=> mX = MX. nX = MX. 0,028/x = 0,91
Do X là kim loại => x thuộc {I; II; III}
x = 1 => MX . 0,028/1 = 0,91 => MX = 32,5 (loại)
x = 2 => MX . 0,028/2 = 0,91 => MX = 65 => X là Zn
x = 3 => MX . 0,028/3 = 0,91 => MX = 97,5 (loại)
Vậy X là kẽm Zn
mHCl = M. n = 36,5. 0,028 = 1,022g
mddHCl = \(\frac{m_{HCl}.100}{C}=\frac{1,022.100}{10}=10,22\)(g)

Gọi kim loại cần tìm là `A` và có hóa trị là `x`
`2A + 2xH_2 O -> 2A(OH)_x + x H_2↑`
`[0,15] / x` `0,075` `(mol)`
`n_[H_2] = [ 1,68 ] / [ 22,4 ] = 0,075 (mol)`
`=>M_A = 3 / [ [ 0,15 ] / x ] = [ 3x ] / [ 0,15]`
`@ x = 1 => M_A = 20 ( g // mol ) ->` Loại
`@ x = 2 => M_A = 40 ( g // mol )->` Nhận và `A` là `Ca`
`@ x = 3 => M_A = 60 ( g // mol )->` Loại
Vậy tên kim loại cần tìm là `Ca`

a) Gọi Kl cần tìm là X có hóa trị chưa biết là n
2X+ 2nHCl = 2XCln+ nH2
Có nH2=0,25 mol --> nX= 0,5/n mol ---> mX=0,5.MX/n=16,25 --> MX=32,5n
n=1 => MX=32,5( không có Kl nào tm)
n=2 => MX=65( Zn)
b) nHCl= 2nH2=2.0,25=0,5 mol
==> VddHCl cần = 0,5/0,2=2,5 lit
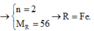
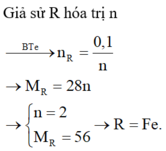
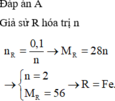
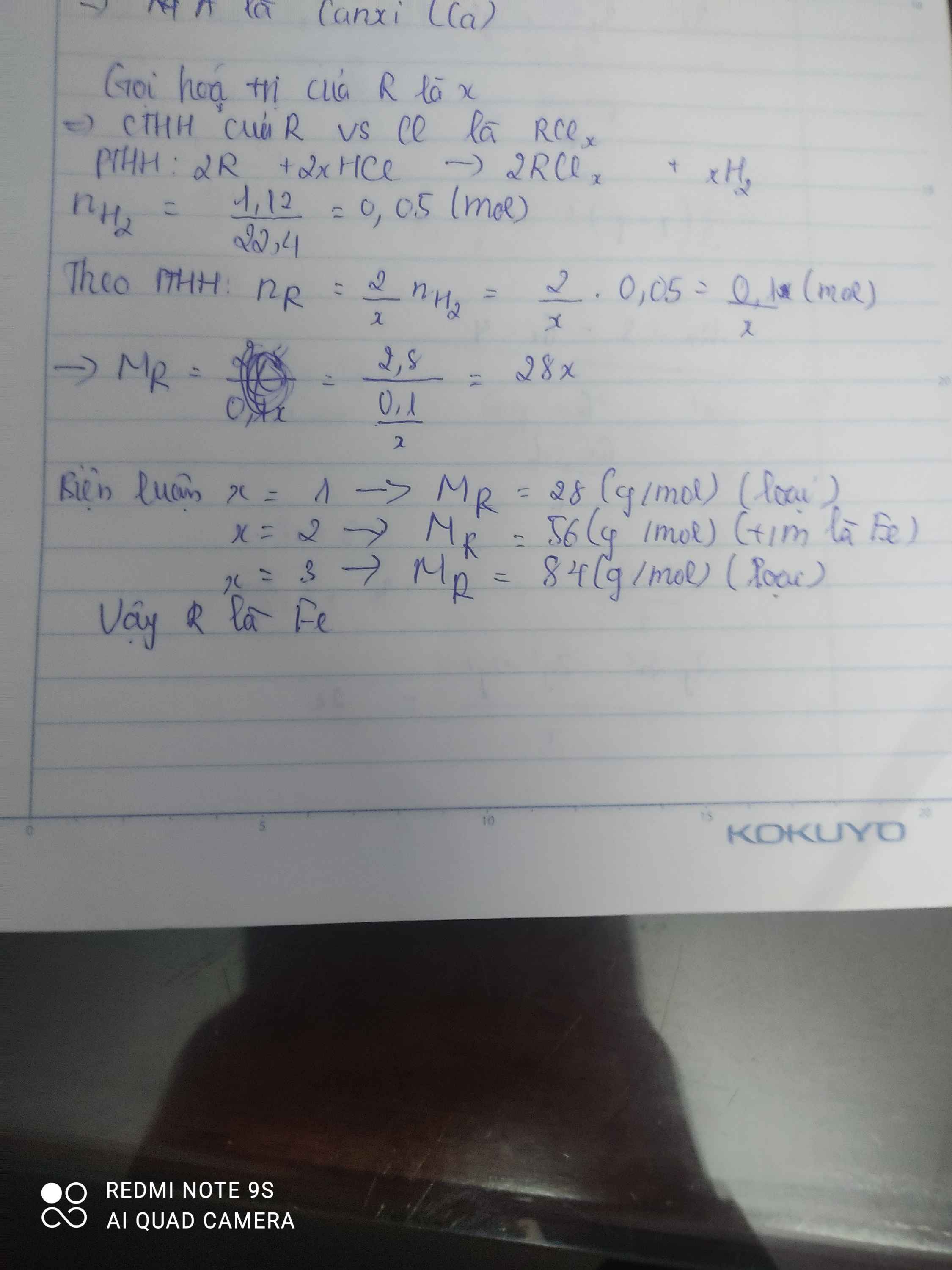
Lâu lắm rồi ms lm 1 bài hóa!
PTHH: 2R + 2xHCl --> 2RClx + xH2
Ta có; nH2 = \(\dfrac{16,8}{22,4}\) = 0,75 mol
Cứ 1 mol R --> x mol H2
2R (g) --> x mol H2
13,5 (g) --> 0,75 mol
=> 0,75.2R = 13,5x
=> R = \(\dfrac{13,5x}{0,75.2}=9x\)
Vì R là kim loại => x = 1 ; 2; 3
Nếu x = 1 => R = 9 (Loại)
Nếu x = 2 => R = 18 (Loại)
Nếu x = 3 => R = 27 ( Al)
=> R là Nhôm ( Al)
Gọi hóa trị của R là x
Theo đề ta có PTHH:
2R + 2xHCl \(\xrightarrow[]{}\) 2RClx + xH2
Theo đề: \(n_{H_2}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\)
Theo PTHH:
\(n_R=\dfrac{2}{x}n_{H_2}=\dfrac{2}{x}\times0,75=\dfrac{1,5}{x}\left(mol\right)\)
=> \(M_R=\dfrac{13,5}{\dfrac{1,5}{x}}=\dfrac{13,5x}{1,5}=9x\) (g/mol)
Ta có bảng sau:
=> R là nhôm (Al) có hóa trị III