Nung m gam đá vôi (CaCO3) một thời gian với hiệu suất 75% thu được 80 gam chất rắn. Tính giá trị của m.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn đáp án C
m C a C O 3 = 0 , 8 m
C a C O 3 ® CaO + C O 2
a a a (mol)
44a = m – 0,78m Þ a = 0,005m
H % = 100 . 0 , 005 m . 100 % 0 , 8 m = 62 , 5 %

lấy m=100g
=> mCaCO3=80 => n=0.8
n pứ=x => mCaO=56x
56x/(56x+(0.8-x)*100+20)=0.4565
=> x=0.6 =|> H=0.6/0.8=0.75=75%

Giả sử có 100g đá
=> \(m_{CaCO_3}=\dfrac{100.80}{100}=80\left(g\right)\)
\(n_{CaCO_3}=\dfrac{80}{100}=0,8\left(mol\right)\)
Gọi số mol CaCO3 phân hủy
PTHH: CaCO3 --to--> CaO + CO2
a-------------->a--->a
=> mY = 100 - 44a (g)
=> mCaO = 56a (g)
=> \(\dfrac{56a}{100-44a}.100\%=45,65\%\)
=> a = 0,6 (mol)
=> \(H=\dfrac{0,6}{0,8}.100\%=75\%\)

\(m_{CaCO_3}=90\%.400=360\left(g\right)\\ \rightarrow n_{CaCO_3}=\dfrac{360}{100}=3,6\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
3,6 ----------> 3,6 -----> 3,6
\(\rightarrow n_{CaO}=3,6.75\%=2,7\left(mol\right)\\ \rightarrow n_{CaCO_3\left(chưa.pư\right)}=3,6-2,7=0,9\left(mol\right)\)
\(\rightarrow m_X=0,9.100+2,7.56=241,2\left(g\right)\\ \%m_{CaO}=\dfrac{0,9.100}{241,2}=37,31\%\)
\(V_Y=V_{CO_2}=3,6.75\%.22,4=60,48\left(l\right)\)
\(m_{CaCO_3}=\dfrac{400\cdot90\%}{100\%}=360g\Rightarrow n_{CaCO_3}=\dfrac{360}{100}=3,6mol\)
\(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
3,6 3,6 3,6
Thực tế: \(n_{CaO}=3,6\cdot75\%=2,7mol\)
\(\Rightarrow m_{CaO}=2,7\cdot56=151,2g\)

mCaCO3 = 500*80%= 400 (g)
nCaCO3 = 400/100 = 4 (mol)
nCaCO3(pư) = 4*70%=2.8 (mol)
CaCO3 -to-> CaO + CO2
2.8..................2.8
Chất rắn X : CaCO3 dư , CaO
mX = ( 4 -2.8 ) *100 + 2.8*56 = 276.8 (g)
%CaO = 2.8*56/276.8 * 100% = 56.64%
a)mCaCO3=500.80%=400(g) -> nCaCO3=400/100=4(mol)
PTHH: CaCO3 -to-> CaO + H2O
nCaO(LT)=nCaCO3=4(mol)
=> nCaO(TT)=4. 70%=2,8(mol)
=>mX=mCaO+ m(trơ)+ mCaCO3(chưa p.ứ)=2,8.56+100+ 1,2.100=376,8(g)
b) %mCaO= (156,8/376,8).100=41,614%

a)mCaCO3=500.80%=400(g) -> nCaCO3=400/100=4(mol)
PTHH: CaCO3 -to-> CaO + H2O
nCaO(LT)=nCaCO3=4(mol)
=> nCaO(TT)=4. 70%=2,8(mol)
=>mX=mCaO+ m(trơ)+ mCaCO3(chưa p.ứ)=2,8.56+100+ 1,2.100=376,8(g)
b) %mCaO= (156,8/376,8).100=41,614%

\(m_{CaCO_3}=400\cdot90\%=360\left(g\right)\)
\(m_{trơ}=400-360=40\left(g\right)\)
\(n_{CaCO_3}=\dfrac{360}{100}=3.6\left(mol\right)\)
\(a.\)
\(n_{CaCO_3\left(pư\right)}=3.6\cdot75\%=2.7\left(mol\right)\)
\(CaCO_3\underrightarrow{^{^{t^0}}}CaO+CO_2\)
\(2.7........2.7...........2.7\)
\(m_X=m_{CaO}+m_{CaCO_3\left(dư\right)}+m_{trơ}=2.7\cdot56+\left(3.6-2.7\right)\cdot100+40=281.2\left(g\right)\)
\(b.\)
\(\%CaO=\dfrac{2.7\cdot56}{281.2}\cdot100\%=53.77\%\)
\(V_{CO_2}=2.7\cdot22.4=60.48\left(l\right)\)
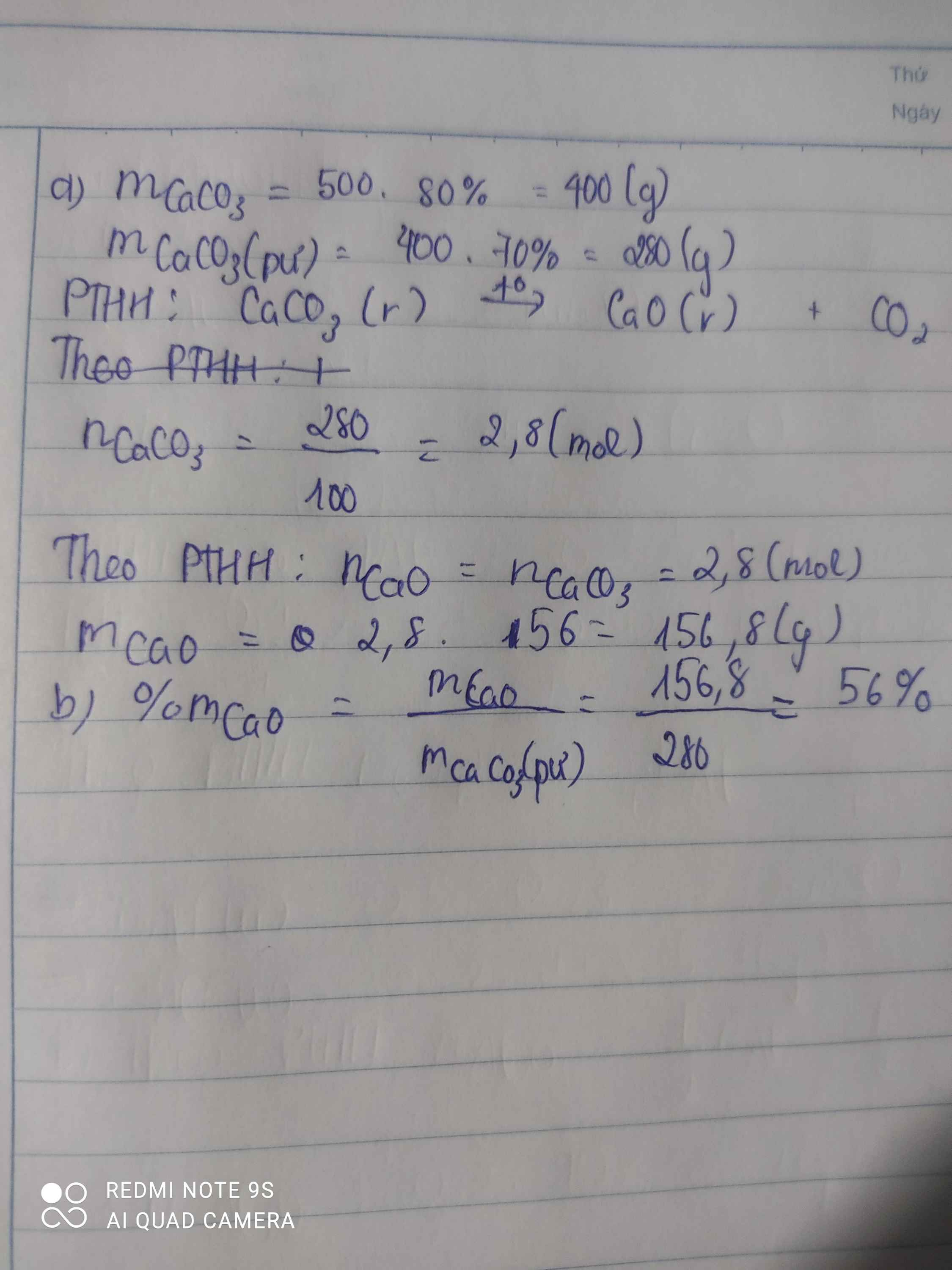
Gọi $n_{CaCO_3} = a(mol)$
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
Theo PTHH :
$n_{CO_2} = n_{CaCO_3\ pư} = 0,75a(mol)$
Bảo toàn khối lượng :
$100a = 80 + 0,75a.44 \Rightarrow a = 1,194(mol)$
$m = 1,194.100 = 119,4(gam)$