Để chuẩn bị cho buổi thí nghiệm thực hành của lớp cần thu 20 lọ khí oxi, mỗi lọ có dung tích 100 ml. Tính khối lượng KMnO4 fải dùng, giả sử khí oxi thu được ở đktc và hao hụt 10%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(V_{O_2}=20.0,1=2\left(l\right)\)
=> \(n_{O_2}=\dfrac{2}{22,4}=\dfrac{5}{56}\left(mol\right)\)
=> nO2(PTHH) = \(\dfrac{5}{56}:90\%=0,1\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,2<------------------------------0,1
=> \(m_{KMnO_4}=0,2.158=31,6\left(g\right)\)
b)
PTHH: \(2KClO_3\xrightarrow[MnO_2]{t^o}2KCl+3O_2\)
\(\dfrac{1}{15}\)<--------------------0,1
=> \(m_{KClO_3}=\dfrac{1}{15}.122,5=8,167\left(g\right)\)

a) \(V_{O_2\left(thu.được\right)}=20.0,1=2\left(l\right)\)
=> \(V_{O_2\left(sinh.ra\right)}=\dfrac{2.100}{90}=\dfrac{20}{9}\left(l\right)\)
=> \(n_{O_2\left(sinh.ra\right)}=\dfrac{\dfrac{20}{9}}{22,4}=\dfrac{25}{252}\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
\(\dfrac{25}{126}\)<----------------------------\(\dfrac{25}{252}\)
=> \(m_{KMnO_4}=\dfrac{25}{126}.158=\dfrac{1975}{63}\left(g\right)\)
b)
PTHH: 2KClO3 --to,MnO2--> 2KCl + 3O2
\(\dfrac{25}{378}\)<---------------------\(\dfrac{25}{252}\)
=> \(m_{KClO_3}=\dfrac{25}{378}.122,5=\dfrac{875}{108}\left(g\right)\)

Bài 6:
PTHH: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{H_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\\n_{O_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,375}{2}>\dfrac{0,125}{1}\) \(\Rightarrow\) H2 còn dư, O2 p/ứ hết
\(\Rightarrow n_{H_2O}=0,25\left(mol\right)\) \(\Rightarrow m_{H_2O}=0,25\cdot18=4,5\left(g\right)\)

a) Do khí oxi thu được hao hụt 10% nên hiệu suất phản ứng là 90%.
Thể tích khí oxi thu được là:
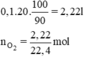
Phương trình hóa học của phản ứng nhiệt phân KMnO4:
2KMnO4 -to→ O2 + K2MnO4 + MnO2.
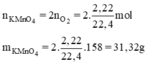
b) Ý b) tách biệt so với ý a), ngoài ra ở ý b) không cho lượng oxi hao hụt là bao nhiêu nên ta lấy hiệu suất phản ứng đạt 100%.
Thể tích khí oxi thu được là: V = 0,1.20 = 2 (lít)


a, Thể tích khí oxi cần thu là: 20*100 = 2000(ml) = 2(l).
Vì hao hụt 10% nên thể tích khí oxi cần có là: 100*2/90 = 20/9 (l).
Số mol khí oxi là: 20/(22,4*9) = 0,099 (mol)
2KMnO4 => K2MnO4 + MnO2 + O2
Số mol KMnO4 là: 0,099 * 2 = 0,2 (mol)
Khối lượng KMnO4 là: 0,2*158 = 31,3 (g)
b, 2KClO3 => 2KCl + 3O2
Số mol KClO3 là: 0,099*2/3 = 0,066 (mol).
Khối lượng cần dùng là: 0,066*122,5 = 8,085 (g)
2 PTPU trên đều có nhiệt độ

a, Thể tích khí oxi cần thu là: 20*100 = 2000(ml) = 2(l).
Vì hao hụt 10% nên thể tích khí oxi cần có là: 100*2/90 = 20/9 (l).
Số mol khí oxi là: 20/(22,4*9) = 0,099 (mol)
2KMnO4 => K2MnO4 + MnO2 + O2
Số mol KMnO4 là: 0,099 * 2 = 0,2 (mol)
Khối lượng KMnO4 là: 0,2*158 = 31,3 (g)
b, 2KClO3 => 2KCl + 3O2
Số mol KClO3 là: 0,099*2/3 = 0,066 (mol).
Khối lượng cần dùng là: 0,066*122,5 = 8,085 (g)
Hihi
Thể tích của O2 là : 20 x 100 =2000 ml = 2l
=> \(n_{O_2}\) = \(\dfrac{2}{22,4}\) = \(\dfrac{5}{56}\)
Vì hao hụt 10% => \(n_{O_2}\) cần có là : \(\dfrac{5}{56}:90\%\) = \(\dfrac{25}{252}\)
PTHH: 2KMnO4 --> K2MnO4 + MnO2 + O2
Theo PT: \(n_{KMnO_4}=2n_{O_2}\) = \(\dfrac{25}{252}\times2\) = \(\dfrac{25}{126}\)
=> \(m_{KMnO_4}\) = \(\dfrac{25}{126}\times158\) = 31,35g
mỗi lọ có thể tích là 100ml thì đúng hơn
Ta có :
mỗi lọ có 0,1(lít) O2 => 20 lọ có : 0,1 . 20 = 2(lít)
=> nO2 = 2 : 22,4 = 0,09(mol)
2KMnO4(0,18) \(\rightarrow\) K2MnO4 + MnO4 + O2(0,9)
=> mKMnO4 = 0,18 . 158 = 28,44(g)
sai thôi nhè