1.Cho 200g dung dịch NaOH 60% hòa tam vào 200g dung dịch NaOH 30%
a) Tính mNaOH
b) Tính m dung dịch NaOH
c) Tính C% NaOH mới
2. Cho 200g NaOH 20% hòa tan vào 400g dung dịch NaOH 30%.
a) Tính mNaOH mới
b) Tính nNaOH mới
c) TÍnh C% NaOH mới
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)\(C\%=\dfrac{m_{ct}}{m_{dd}}\cdot100\%=\dfrac{5}{5+45}\cdot100\%=10\%\)
b)\(C\%=\dfrac{m_{ct}}{m_{dd}}\cdot100\%=\dfrac{5,6}{5,6+94,4}\cdot100\%=5,6\%\)
c)\(m_{ctNaOH}=\dfrac{200\cdot10\%}{100\%}=20g\)
\(m_{ctNaOH}=\dfrac{300\cdot5\%}{100\%}=15g\)
\(C\%=\dfrac{m_{ct}}{m_{dd}}\cdot100\%=\dfrac{20+15}{200+300}\cdot100\%=7\%\)
\(a,C\%_{NaOH}=\dfrac{5}{5+45}=10\%\)
b, \(n_{CaO}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: CaO + H2O ---> Ca(OH)2
0,1 ---------------> 0,1
\(\rightarrow C\%_{Ca\left(OH\right)_2}=\dfrac{74.0,1}{5,6+94,4}=37\%\)
c, \(m_{NaOH}=10\%.200+5\%.300=35\left(g\right)\)
\(\rightarrow C\%_{NaOH}=\dfrac{35}{200+300}=7\%\)

\(a,C\%_{CuSO_4}=\dfrac{5}{200+5}.100\%=2,43\%\\ b,C\%_{NaOH}=\dfrac{0,2.40}{200}.100\%=4\%\\ c,n_{NH_3}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ C\%_{NH_3}=\dfrac{0,3.17}{200+0,3.17}.100\%=2,5\%\\ d,n_{KCl}=\dfrac{9.10^{22}}{6.10^{23}}=0,15\left(mol\right)\\ C\%_{KCl}=\dfrac{0,15.74,5}{200}=5,5875\%\)

a) mNaOH= 200.10%=20(g)
b) nNaOH=0,4(mol)
=>CMddNaOH=0,4/0,2=2(M)

Gọi lượng NaOH cần hòa tan vào dd A là x (g)
Ta có công thức :
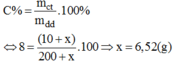
Vậy phải trộn thêm 6,52g NaOH vào dung dịch A để được dung dịch A để được dung dịch NaOH 8%.

\(n_{CO_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ n_{NaOH}=\dfrac{m}{M}=\dfrac{m_{dd}.C\%}{M}=\dfrac{200.16\%}{40}=0,8\left(mol\right)\)
Có: \(\dfrac{n_{NaOH}}{n_{CO_2}}=4\)
=> Phản ứng tạo muối Na2CO3
PT:
\(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
0,2. 0,4 0,2
=> dd sau phản ứng có những chất tan là:
\(\left\{{}\begin{matrix}Na_2CO_3:0,2\left(mol\right)\\NaOH:0,4\left(mol\right)\end{matrix}\right.\)
mdd spu=0,2.44+200=208,8(g)
\(\%m_{NaOH}=\dfrac{0,4.40}{208,8}.100\%=7,66\%\\\%m_{Na_2CO_3}=\dfrac{0,2.106}{208,8}.100\%=10,15\% \)
Câu 1:
nAl= 0,1(mol)
PTHH: 2Al + 6 HCl -> 2 AlCl3 + 3 H2
nAlCl3= nAl=0,1(mol)
-> mAlCl3= 133,5 x 0,1= 13,35(g)
mddAlCl3= mAl + mddHCl - mH2 = 2,7 + 200 - 3/2 x 0,1 x 2= 202,4(g)
C%ddAlCl3= (13,35/202,4).100= 6,596%

a, \(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
\(m_{NaOH}=0,2.40=8\left(g\right)\)
b, \(n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
\(c,C\%=\dfrac{6}{200}.100\%=3\%\)
\(m_{NaCl}=\dfrac{200.8}{100}=16\left(g\right)\)
Câu 1: Từ 200g dd NaOH 60%
=> mct1=\(\dfrac{C\%.m_{dd}}{100\%0}=\dfrac{60.200}{100}=120\left(g\right)\)
Từ 200 g dd NaOH 30%
=> mct2=\(\dfrac{C\%.m_{dd}}{100\%}=\dfrac{30.200}{100}=60\left(g\right)\)
Vậy \(m_{NaOH\left(mới\right)}=m_{ct1}+m_{ct2}=120+60=180\left(g\right)\)
b) md d NaOH=md d1 + md d2= 200 +200 =400(g)
c) \(C\%_{NaOH}=\dfrac{m_{NaOH}.100\%}{m_{ddNaOH}}=\dfrac{180.100}{400}=45\left(\%\right)\)
Câu 2: Từ 200g dd NaOH 20%
=> mct1=\(\dfrac{C\%.m_{dd}}{100\%0}=\dfrac{20.200}{100}=40\left(g\right)\)
Từ 400 g dd NaOH 30%
=> mct2=\(\dfrac{C\%.m_{dd}}{100\%}=\dfrac{30.400}{100}=120\left(g\right)\)
Vậy \(m_{NaOH\left(mới\right)}=m_{ct1}+m_{ct2}=40+120=160\left(g\right)\)
b) md d NaOH=md d1 + md d2= 200 +400 =600(g)
c) \(C\%_{NaOH}=\dfrac{m_{NaOH}.100\%}{m_{ddNaOH}}=\dfrac{160.100}{600}\approx27\left(\%\right)\)