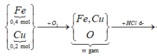
Đốt nóng 40,6 g hỗn hợp hai kim loại Al và Zn trong bình đựng khí oxi, sau một thời gian, ngừng đốt nóng, để nguội, thu được 48,6 g hỗn hợp gồm 4 chất rắn. Cho hỗn hợp rắn này tan hết vào dung dịch HCl thì được 10,08 lít H2.
a) Viết phương trình hóa học của các phản ứng
b) Xác định % khối lượng Al và Zn trong hỗn hợp đầu
(Đề thi chọn đội tuyển hóa 9 năm học 2014-2015 trường THPT chuyên Trần Đại Nghĩa).

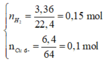
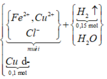
 Cho em hỏi tại sao nhân 2 mà không phải nhân 4 ạ ?
Cho em hỏi tại sao nhân 2 mà không phải nhân 4 ạ ?
a , PTHH :
2Zn + O2 -> 2ZnO
a..........0,5a......a
4Al + 3O2 -> 2Al2O3
b............0,75b.........0,5b
Zn + 2HCl -> ZnCl2 + H2
(1-a)..............................(1-a)
2Al + 6HCl -> 2AlCl3 + 3H2
ZnO + 2HCl -> ZnCl2 + H2O
Al2O3 + 6HCl -> 2AlCl3 + 3H2O
b , tạm thời bây h mik chưa đánh máy kịp , phone chụp nhưng ko up lên được , nếu sáng mai chưa có lời giải , có thể mai mik up lên nha ^^
a,PTHH
4Al + 3O2 -> 2Al2O3
m......0,75m.......0,5m
2Zn + O2 -> 2ZnO
n..........0,5n......n
Al2O3 + 6HCl -> 2AlCl3 + 3H2O
0,5m........3m...........m.............1,5m
ZnO + 2HCl -> ZnCl2 + H2O
n..........2n.............n...............n
2Al + 6HCl -> 2AlCl3 + 3H2
(a-m)...............................................1,5(a-m)
Zn + 2HCl -> ZnCl2 + H2
(b-n).....................................(b-n)
b , Gọi a,b lần lượt là số mol Al , Zn trong hỗn hợp
m , lần lượt là số mol Al , Zn tham gia phản ứng với oxi
Theo bài ra : 27a+ 65b= 40,6 (1)
Theo đề bài 51m+ 81n+ 27(a-m)+ 65(b-n)=48,6 - tong khối luong 4 chat răn sau phan ung
<=> 8(3m+2n)=8=> 3m+2n=1 ( cái này giải phương trình thông thường thôi , mik làm tắt)
nH2 = 10,08/22,4=0,45(mol)
=> 1,5(a-m)+b-n=0,45
=> 2( 1,5a-1,5m+b-n) = 0,9
=> 3a+2b -(3m+2n)= 0,9
=> 3a+2b=1,9 (2)
Từ (1) và (2) ta có hệ
\(\left\{{}\begin{matrix}27a+65b=40,6\\3a+2b=1,9\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,3\\b=0,5\end{matrix}\right.\)
Tới đây thì ok rồi , bạn tự làm phần còn lại nhé
chúc bạn học tốt , sorry vì mik up muộn ^^