5. (VD) Trộn 200 ml dung dịch H2SO4 0,5M với 150ml dung dịch NaOH xM. Sau khi phản ứng xảy ra hoàn toàn nhỏ vào vài giọt phenolphtalein thấy dung dịch chuyển sang màu hồng. Thêm từ từ H2SO4 0,5M vào cho đến khi dung dịch mất màu thì đã sử dụng 50ml dung dịch axit. Tìm x.7. (VD) Hoà tan hoàn toàn 16,25 gam một kim loại hoá trị II bằng dung dịch HCl 18,25% thu được 5,6 lít khí H2 (đktc).a) Xác định kim loại.b) Tính khối lượng...
Đọc tiếp
5. (VD) Trộn 200 ml dung dịch H2SO4 0,5M với 150ml dung dịch NaOH xM. Sau khi phản ứng xảy ra hoàn toàn nhỏ vào vài giọt phenolphtalein thấy dung dịch chuyển sang màu hồng. Thêm từ từ H2SO4 0,5M vào cho đến khi dung dịch mất màu thì đã sử dụng 50ml dung dịch axit. Tìm x.
7. (VD) Hoà tan hoàn toàn 16,25 gam một kim loại hoá trị II bằng dung dịch HCl 18,25% thu được 5,6 lít khí H2 (đktc).
a) Xác định kim loại.
b) Tính khối lượng dung dịch HCl đã dùng.
c) Tính nồng độ phần trăm của dung dịch muối sau phản ứng.
8. (VD) Hoà tan 10 (g) CaCO3 vào 114,1 gam dung dịch HCl 8%.
a) Viết PTHH xảy ra.
b) Tính nồng độ phần trăm các chất trong dung dịch sau phản ứng.
9. (VD) Từ 80 tấn quặng pirit chứa 40% lưu huỳnh, người ta sản xuất được 73,5 tấn axit sunfuric.
a) Viết các PTHH để sản xuất axit sunfuric từ lưu huỳnh.
b) Tính hiệu suất của quá trình sản xuất.
c) Tính khối lượng dung dịch axit sunfuric 50% thu được từ 73,5 tấn H2SO4 được sản xuất ở trên.
10. (VD) Hoà tan 2,5 gam một mẩu quặng Dolomit với thành phần chính là CaCO3 và MgCO3, còn lại là các tạp chất trơ. Hoà tan hoàn toàn mẩu quặng trên trong dung dịch HCl dư thu được 0,448 lít khí (đktc) và dung dịch chứa 2,14 gam muối. Xác định thành phần phần trăm các muối cacbonat trong mẩu quặng.
11. (VDC) Để hoà tan vừa đủ 4,75 gam hỗn hợp Zn và Fe cần sử dụng V (lít) dung dịch hỗn hợp HCl 0,5M và H2SO4 0,75M, thu được 1,792 lít khí (đktc).
a) Xác định phần trăm về khối lượng các kim loại trong hỗn hợp.
b) Tìm V.

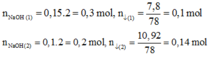


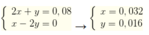
Rót 50 ml dung dịch H2SO4 2M vào bình chứa 100 ml dung dịch NaOH 3M và khuấy đều. Sau đó, nhỏ 2 - 3 giọt dung dịch phenolphtalein vào bình phản ứng. Hiện tượng xảy ra là gì?
A. Xuất hiện kết tủa màu trắng.
B. Hình thành bọt khí không màu.
C. Dung dịch từ không màu xuất hiện màu hồng.
D. Không có hiện tượng gì xảy ra.
---
nH2SO4= 0,05.2=0,1(mol)
nNaOH=0,1.3=0,3(mol)
PTHH: 2 NaOH + H2SO4 -> Na2SO4 + 2 H2O
Vì 0,3/2 > 0,1/1
=> NaOH dư, H2SO4 hết => nhỏ phenolphtalein vào xuất hiện màu hồng
=> CHỌN C
C