Đốt cháy hoàn toàn 1 lượng bột Y ttong oxi thi thu được chất rắn có khối lượng lớn hơn 25% khối lượng kim loại ban đầu . Xác định Y
mong các bạn giải giúp minh mình sap di thi
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(M+H_2O\rightarrow MOH+\dfrac{1}{2}H_2\\ m_{H_2}=2,3-2,2=0,1\left(g\right)\Rightarrow n_{H_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ n_M=2.0,05=0,1\left(mol\right)\\ M_M=\dfrac{2,3}{0,1}=23\left(\dfrac{g}{mol}\right)\\ \Rightarrow M\left(I\right):Natri\left(Na=23\right)\)

Giả sử có 1 mol Cu
=> mCu(bd) = 64 (g)
\(hh_{sau.pư}=64+\dfrac{1}{6}.64=\dfrac{224}{3}\left(g\right)\)
Gọi số mol Cu pư là a (mol)
PTHH: 2Cu + O2 --to--> 2CuO
a---------------->a
=> hh sau pư chứa \(\left\{{}\begin{matrix}CuO:a\left(mol\right)\\Cu:1-a\left(mol\right)\end{matrix}\right.\)
=> \(80a+64\left(1-a\right)=\dfrac{224}{3}\)
=> a = \(\dfrac{2}{3}\left(mol\right)\)
\(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{64\left(1-\dfrac{2}{3}\right)}{\dfrac{224}{3}}.100\%=28,57\%\\\%m_{CuO}=\dfrac{80.\dfrac{2}{3}}{\dfrac{224}{3}}.100\%=71,43\%\end{matrix}\right.\)

PTHH: 2A + O2 → 2AO
Khối lượng oxit thu được là:
a . ( 100% + 40% ) = 1,4a
Số mol của kim loại A tính theo khối lượng là: a/MA
Số mol của oxit kim loại A là: 1,4a/MA + 16
Mà số mol của A = số mol của AO
=> a/MA = 1,4a/MA + 16
<=> aMA + 16a = 1,4aMA
Gút gọn a ở 2 bên của phương trình ta được:
<=> MA + 16 = 1,4MA
<=> 0,4MA = 16
<=> MA = 40 ( Canxi)
PTHH: 2Ca + O2 → 2CaO

Đặt nZn = x mol; nFe = y mol.
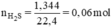
Ta có hệ phương trình: 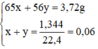
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g

\(n_{Al} = a ; n_{Fe} = b\Rightarrow 27a + 56b = 27,6(1)\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 0,5a(mol)\\ n_{Fe_3O_4} = \dfrac{1}{3}n_{Fe} = \dfrac{b}{3}(mol)\\ \Rightarrow 0,5a.102 + \dfrac{b}{3}232 = 43,6(2)\\ (1)(2) \Rightarrow a = 0,4 ; b = 0,3\\ m_{Al} = 0,4.27 = 10,8(gam) ; m_{Fe} = 0,3.56 = 16,8(gam)\)

Câu 1:
a, \(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
b, \(n_{C_2H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{CO_2}=2n_{C_2H_2}=0,6\left(mol\right)\)
\(\Rightarrow m_{CO_2}=0,6.44=26,4\left(g\right)\)
c, \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=0,6\left(mol\right)\Rightarrow m_{CaCO_3}=0,6.100=60\left(g\right)\)
Câu 2:
a, Gọi CTHH cần tìm là FexOy.
Ta có: \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
Mà: mFe + mO = 32 ⇒ mO = 32 - 22,4 = 9,6 (g)
\(\Rightarrow n_O=\dfrac{9,6}{16}=0,6\left(mol\right)\)
⇒ x:y = 0,4:0,6 = 2:3
→ CTHH có dạng (Fe2O3)n
\(\Rightarrow n=\dfrac{160}{56.2+16.3}=1\)
Vậy: Oxit sắt là Fe2O3
b, PT: \(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=\dfrac{3}{2}n_{Fe}=0,6\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,6.100=60\left(g\right)\)

a) Gọi số mol Al, Zn là 2a, a (mol)
PTHH: 4Al + 3O2 --to--> 2Al2O3
2a-->1,5a---------->a
2Zn + O2 --to--> 2ZnO
a---->0,5a------->a
=> \(102a+81a=18,3\)
=> a = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{0,2.27+0,1.65}.100\%=45,378\%\\\%m_{Zn}=\dfrac{0,1.65}{0,2.27+0,1.65}.100\%=54,622\%\end{matrix}\right.\)
b) \(n_{O_2}=1,5a+0,5a=0,2\left(mol\right)\)
=> \(V_{O_2}=0,2.22,4=4,48\left(l\right)\)
Phần lớn hơn chính là oxi trong oxit kim loại.
TH1: Oxit Y có công thức: \(Y_3O_4\)
\(\Rightarrow\dfrac{16.4}{3Y}=0,25\)
\(\Leftrightarrow Y=85,333\left(l\right)\)
TH2: Oxit Y có công thức \(Y_2O_x\)
\(\Rightarrow\dfrac{16x}{2Y}=0,25\)
\(\Leftrightarrow Y=32x\)
Thế x lần lược các giá trị 1, 2, 3, .. ta nhận \(\left\{{}\begin{matrix}x=2\\Y=64\end{matrix}\right.\)
Vậy Y là Cu và công thức oxit viết lại là: \(CuO\)
@Minh Tuấn Lê Quang ô hình như bài này của lớp 8 à ?