Bài1 : Cho lượng khí CuO đi qua 1,6 g CuO và nung nóng sau p/ư với hiệu suất 80% thu đc hỗn hợp chất rắn A . Tính khối lượng chất rắn A
Bài 2 : Trong một bình kín chứa 2 mol O2 , 3 mol SO2 và một ít bột súc tác . Nung nóng bình 1 thời gian thu đc hỗn hợp khí B . Nếu H p/ư là 75% thì có bao nhiêu mol SO3 tạo thành . Nếu tổng số mol các khí trong B là 4,25 mol . Tính H p/ ư
Bài 3 : Với 500 g đá vôi chứa 80% CaCO3 ( phần còn lại là chất trơ ) sau một thời gian thu đc chất rắn X biết H =70% . Tính thành phần % khối lượng CaO trong chất rắn X
Bài 4 : Người ta tiến hành điện phân nóng chảy quặng oxit loại quạng này chứa chủ yếu là nhôm oxit sau p/ư thu đc nhôm và oxi . Nếu dùng quặng oxit chứa 50% nhôm oxi để sản sưất 108 g nhôm thì quặng đen dùng bao nhiêu . Biết H là 85%
Bài 5 : Cho lượng khí H2 đi qua ống thủy tinh chứa 20 g bột ở 400 độ C sau phản ứng thu đc 16,8 g chất rắn . Nêu hiện tượng phản ứng xảy ra . Tính hiệu suất p/ ư . Tính thể tích H2 (đktc) tham gia p/ư



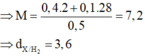
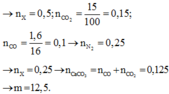

Bài 3 :
\(mCaCO_3=\dfrac{500.80}{100}=400(g)\)
\(=> m tạp chất = 100(g)\)
\(=> nCaCO_3=\dfrac{400}{100}=4(mol)\)
\(PTHH:\) \(CaCO_3-t^o-> CaO+CO_2\)
Theo PTHH: \(nCaO=nCaCO_3=4(mol)\)
\(=> mCaO(lí thuyết)=4.56=224(g)\)
Vì \(H=70\%\)
\(=> mCaO(thực tế)=\dfrac{224.70}{100}=156,8(g)\)
Chất rắn X gồm tạp chất (chất trơ) và CaO
Thành phần phần trăm khối lượng CaO trong X là
\(\%mCaO=\dfrac{156,8.100}{156,8+100}=61,069\%\)
Bài 4 :
\(PTHH:\) \(2Al_2O_3-đpnc-> 4Al+3O_2\)
\(nAl=\dfrac{108}{27}=4(mol)\)
Theo PTHH: \(nAl_2O_3(lí thuyết)=2(mol)\)
\(=> mAl_2O_3(lí thuyết) = 2.102=204(g)\)
Vì \(H=85\%\)
\(=> mAl_2O_3(thực tế)=\dfrac{204.100}{85}=240(g)\)
Vì trong quặng đen, Al2O3 chỉ chiếm 50%
\(=> mQuặng=\dfrac{240.100}{50}=480(g)\)
Vậy để sản xuất 108g Al cần dùng 480g quặng đen