khử hoàn toàn á (g) Fe2O3 bằng khí H2 dư thu được b(g) kim loại Fe đốt cháy hết lượng Fe này trong khí O2 dư thu dc 23,2g Fe3O4 . hãy viết pthh và tính a,b
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(Fe_2O_3\left(0,15\right)+3H_2\rightarrow2Fe\left(0,3\right)+3H_2O\)
\(3Fe\left(0,3\right)+2O_2\rightarrow Fe_3O_4\left(0,1\right)\)
\(n_{Fe_3O_4}=\frac{23,2}{232}=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=0,15.160=24\left(g\right)\)
\(\Rightarrow m_{Fe}=0,3.56=16,8\left(g\right)\)
Ta có: \(n_{Fe_3O_4}=\frac{23,2}{232}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 -to-> 2Fe + 3H2O (1)
3Fe + 2O2 -to-> Fe3O4 (2)
Theo các PTHH và đề bài, ta có:
\(n_{Fe\left(2\right)}=3.n_{Fe_3O_4\left(2\right)}=3.0,1=0,3\left(mol\right)\)
\(n_{Fe\left(1\right)}=n_{Fe\left(2\right)}=0,3\left(mol\right)\)
\(n_{Fe_2O_3\left(1\right)}=\frac{n_{Fe\left(1\right)}}{2}=\frac{0,3}{2}=0,15\left(mol\right)\)
Ta có: \(a=m_{Fe_2O_3\left(1\right)}=0,15.160=24\left(g\right)\)
\(b=m_{Fe\left(1\right)}=0,3.56=16,8\left(g\right)\)

nFe = 16,8 : 56 = 0,3 (mol)
pthh :3 Fe + 2O2 -t--> Fe3O4
0,3--------------> 0,1 (mol)
=> mFe3O4 =0,1 . 232 = 23,2(G)
nH2 = 44,8 : 22,4 = 2 (g)
pthh : Fe3O4 + H2 -t--> Fe + H2O
LTL : 0,1 / 1 < 2 /1
=> H2 du
nH2 (pu) = nFe3O4 = 0,1 (mol)
=> nH2 (d) = 2-0,1 = 1,9 (mol)
mH2 (d) = 1,9 . 2 = 3,8 (g)

nFe = 2.8/56 = 0.05 (mol)
nO2 = 22.4 / 22.4 = 1 (mol)
3Fe + 2O2 -to-> Fe3O4
0.05__1/30______1/60
mO2 (dư) = ( 1 - 1/30) * 32 = 30.93 (g)
mFe3O4 = 1/60 * 232 = 3.867 (g)
a/ \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b/ Ta có: \(n_{Fe}=\dfrac{2.8}{56}=0.05\left(mol\right)\)
\(n_{O_2}=\dfrac{22.4}{22.4}=1\left(mol\right)\)
Ta có: \(\dfrac{n_{Fe\left(bra\right)}}{n_{Fe\left(pt\right)}}=\dfrac{0.05}{3}=0.016< \dfrac{n_{O_2\left(bra\right)}}{n_{O_2\left(pt\right)}}=\dfrac{1}{2}=0.5\)
=> Oxi phản ứng dư
mO2 dư = (1 - 1/30) . 32 = 30.93 (g)
mFe3O4 = 1/60 . 232 = 3.867 (g)

Đáp án C
(FeO, Fe2O3, Fe3O4) + CO → Fe + CO2
CO2 + Ca(OH)2 dư → a gam ↓ CaCO3
Fe + HCl dư → V lít H2↑
• nFe = nH2 = V/22,4 mol; nCO = nCO2 = a/100 mol.
Theo bảo toàn khối lượng mhỗn hợp oxit = mFe + mCO2 - mCO
→ m = V/22,4 × 56 + a/100 × 44 - a/100 × 28 = 2,5V - 0,16a

Câu 13:
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ PTHH:R_2O_3+3H_2\underrightarrow{t^o}2R+3H_2O\\ Theo.pt:n_{R_2O_3}=\dfrac{1}{3}n_{H_2}=\dfrac{1}{3}.0,3=0,1\left(mol\right)\\ M_{R_2O_3}=\dfrac{16}{0,1}=160\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow2R+16.3=160\\ \Leftrightarrow R=56\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow R.là.Fe\\ CTHH:Fe_2O_3\)
Bài 14:
\(n_{H_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\\ PTHH:Fe+H_2SO_{4\left(loãng\right)}\rightarrow FeSO_4+H_2\uparrow\left(1\right)\\ Theo.pt\left(1\right):n_{Fe}=n_{H_2}=0,125\left(mol\right)\\ PTHH:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\left(2\right)\\ Theo.pt\left(2\right):n_{Fe_2O_3}=\dfrac{1}{3}n_{Fe}=\dfrac{1}{3}.0,125=\dfrac{1}{24}\left(mol\right)\\ m=m_{Fe_2O_3}=\dfrac{1}{24}.160=\dfrac{20}{3}\left(g\right)\\ n=n_{Fe}=0,125.56=7\left(g\right)\)

MX= 19.2=38
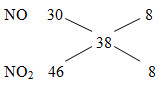
=> nN2=nNO2=x
mFe + mO = moxit
=> mO = moxit- mFe = 7,36-5,6=1,76 gam
=> nO = 0,11 mol
Fe0 →Fe3+ + 3e
0,1 0,3
O0 +2e →O2- N+5 + 3e → N+2 N+5 +1e → N+4
0,11 0,22 3x x x x
Bảo toàn e: 0,3 = 0,22+3x+x =0,22+4x =>x= 0,02
=> nkhí = 2x=0,04 mol
=> Vkhí = 0,04.22,4=0,896 lít=896 ml

PTHH:
Fe2O3 + 3H2 --> (nhiệt độ) 2Fe + 3H2O (1)
3Fe + 2O2 --> ( nhiệt độ) Fe3O4 (2)
nFe3O4=23.2 : 232 = 0.1 (mol)
PTHH (2) => nFe= 3nFe3O4 = 0.1 * 3 = 0.3 (mol)
=> b = mFe= 0.3*56 = 16.8 (g)
PTHH (1) => nFe= 2nFe3O4= 0.3 : 2 = 0.15 (mol)
=> a = mFe2O3 = 0.15 * 160 = 24 (g)
mơn