Người ta khử FexOy ở nhiệt độ cao bằng Al, nếu tỉ lệ khối lượng Fe và Al2O3 tạo thành là 63:51 thì công thức của oxit sắt là gì
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

mgiảm = mO(oxit) = 4.8 (g)
nO = 4.8/16 = 0.3 (mol)
nFexOy = 0.3/y (mol)
MFexOy = 16/0.3/y = 160y/3 (g/mol)
=> 56x + 16y = 160y/3
=> 56x = 112y/3
=> x / y = 2 / 3
CT : Fe2O3

Đáp án C
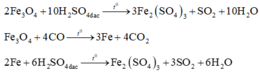
Coi oxit sắt ban đầu là hỗn hợp gồm Fe và O với nFe = a và nO = b.

Với lần thí nghiệm thứ nhất, có sự tham gia của O. Áp dụng định luật bảo toàn mol electron, ta có:
![]()
Với lần thí nghiệm thứ hai, không có sự tham gia của O. Áp dụng định luật bảo toàn mol
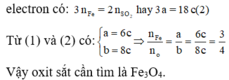

Đáp án C
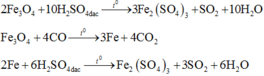
Coi oxit sắt ban đầu là hỗn hợp gồm Fe và O với nFe = a và nO = b.
Gọi thì ![]()
Các quá trình nhường và nhận electron diễn ra như sau:
Quá trình nhường electron:



Đáp án C
Phản ứng của oxit + CO thực chất là:
CO + [O] → CO2
=> mchất rắn giảm = mO pứ = 4,8g => nO = 4,8 : 16 = 0,3 mol
=> mFe = mOxit – mO = 16 – 4,8 = 11,2 => nFe = 11,2 : 56 = 0,2 mol
=> nFe : nO = 0,2 : 0,3 = 2 : 3
=> Oxit là Fe2O3
3FexOy + 2yAl \(\rightarrow\) yAl2O3 + 3xFe
Có : \(\dfrac{m_{Fe}}{m_{Al2O3}}=\dfrac{63}{51}\)
\(\Rightarrow\dfrac{n_{Fe}}{n_{Al2O3}}.\dfrac{M_{Fe}}{M_{Al2O3}}=\dfrac{63}{51}\)
\(\Rightarrow\dfrac{n_{Fe}}{n_{Al2O3}}.\dfrac{56}{102}=\dfrac{63}{51}\Rightarrow\dfrac{n_{Fe}}{n_{Al2O3}}=\dfrac{9}{4}\)
Vậy đặt nFe = 9a(mol) => nAl2O3 = 4a(mol)
Theo PT => nFexOy = 1/x . nFe = 1/x . 9a = 9a/x (mol)
Theo PT => nFexOy = 3/y . nAl2O3 = 3/y . 4a =12a/y (mol)
Do đó : 9a/x = 12a/y
=> x : y = 9a : 12a =3:4
=> x = 3 và y = 4
Vậy CTHH của oxit sắt là Fe3O4