Hòa tan 4,25 g một muối halogen của kim loại kiềm vào dd AgNO3 dư thu được 14,35 kết tủa.Công thức muối là gì
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Định làm mà thấy bên dưới có bài y hệt nên thôi nhé
Mà bạn này..Mk thấy mấy bài này kiểu ở lớp 8,9 mà..Sao bạn cứ để ở lớp 10 thế

Chúc bạn học tốt :))

Đáp án C
![]()
nAgCl = 18,655/143,5 = 0,13
⇒ M= 6,645/ 0,13 - 35,5 = 15,61
⇒ M1 = 9 (Li) < 15,61 < M2 = 23(Na)

Gọi CTTQ của muối halogen là MX
PTHH MX + AgNO3 ----> AgX + MNO3
ta có số mol của MX = số mol của AgX
=> \(\dfrac{4,25}{M+X}\)=\(\dfrac{14,35}{108+X}\) <=> 459+4,25X=14,35M+14,35X
<=> 14,35M+10X=459
+ nếu X là Flo thì M=19(kali)
+ nếu X là Clo thì M=7,24 (loại)
tương tự ta bạn tính ra sẽ loại luôn Brom và Iot
vậy muối halogen đó là KF

0ml-->0,7175g kt
=>200ml--> 14,35g kt.
Đặt ct muối halogen là MX (M là kl kiềm,X là ngto halogen).
MX + AgNO3 = MNO3 + AgX
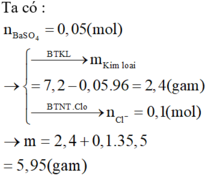
Ta có :
4,25/( M + X ) = 14,35/( 108 + X )
=> M = 4,25 ( 108 + X ) /14,35 - X.
X - tao được kết quả
=> X là 1 trong 3 ngto Cl, Br, I
Thấy lần lượt X={35,5; 80; 127} vào :
=> chỉ có Cl thoa
=> M = 7 ( Liti )
=> CT muối là LCl.
nLCl = 0,1
=> CM = 0,1/0,2
= 0,5 M.

CTHH của muối : RSO4
\(n_{BaSO_4}=\dfrac{2.33}{233}=0.01\left(mol\right)\)
\(RSO_4+BaCl_2\rightarrow RCl_2+BaSO_4\)
\(0.01......................................0.01\)
\(M_{RSO_4}=\dfrac{1.6}{0.01}=160\)
\(\Rightarrow R=160-96=64\left(\dfrac{g}{mol}\right)\)
\(R:Cu\)
\(CT:CuSO_4\)

Đáp án C
Hướng dẫn Ta có: ![]()
![]() Cl + AgNO3 →
Cl + AgNO3 → ![]() NO3 + AgCl
NO3 + AgCl
0,13 mol 0,13 mol
=> (![]() + 35,5).0,13 = 6,645 →
+ 35,5).0,13 = 6,645 → ![]() = 15,62
= 15,62
Mà 2 kim loại kiềm thuộc hai chu kì kế tiếp nhau → Li (7) và Na(23)
gọi CTTQ của muối halogen là MX
PTHH MX + AgNO3 ----> AgX + MNO3
ta có số mol của MX = số mol của AgX
=> \(\dfrac{4,25}{M+X}\)=\(\dfrac{14,35}{108+X}\) <=> 459+4,25X=14,35M+14,35X
<=> 14,35M+10X=459
+ nếu X là Flo thì M=19(kali)
+ nếu X là Clo thì M=7,24 (loại)
tương tự ta bạn tính ra sẽ loại luôn Brom và Iot
vậy muối halogen đó là KF
Ra 10.1X ms đúng. Vậy ct là LiCl