13/ đốt cháy 21g một mẫu sắt không tinh khiết trong oxi dư ng ta thu đc 23,2g oxit sắt từ Fe3O4. tính độ tinh khiết của mẫu sắt đã dùng
16/ tính số mol khí sunfuro sinh ra trong mỗi trường hợp sau
a/ có 1,5 mol khí oxi tham gia phản ứng vs S
b/ đốt cháy hoàn toàn 38,4g S trong khí oxi.

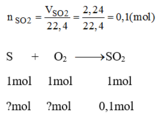
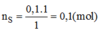
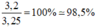
13) \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(n_{Fe_3O_4}=\frac{23,2}{232}=0,1mol\)
\(n_{Fe}=3.n_{Fe_3O_4}=3.0,1=0,3mol\)
\(m_{Fe\left(tinhkhiết\right)}=0,3.56=16,8g\)
Độ tinh khiết là: \(\frac{16,8}{21}.100\left(\%\right)=80\%\)
16) a) S+O2=to=>SO2
\(n_{O_2}=n_{SO_2}=1,5mol\)
b) S+O2=to=>SO2
\(n_S=\frac{38,4}{32}=1,2mol\)
\(n_{SO_2}=n_S=1,2mol\)