Đun nóng 1 chiếc lò so mỏng bằng nhôm có khối lượng là 15,12(g) trong Oxi trong khoảng thời gian ngắn, khi phản ứng kết thúc chiếc lò so thu đc có khối lượng là 17,25(g)
a) Viết phương trình hoá học xảy ra?
b) Trong thời gian đun nóng chiếc lò xo Al đã phản ứng hoàn toàn với Oxi chưa ? Nếu Al chưa phản ứng hết hãy tính % lượng Al đã phản ứng với Oxi?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a.2Fe_2O_3+3C\xrightarrow[t^0]{}4Fe+3CO_2\\ 2CuO+C\xrightarrow[t^0]{}2Cu+CO_2\\ b.n_{CO_2}=\dfrac{11,2}{22,4}=0,5mol\\ n_{Fe_2O_3}=a;n_{CuO}=b\\ \Rightarrow\left\{{}\begin{matrix}160a+80b=64\\1,5a+0,5b=0,5\end{matrix}\right.\\ \Rightarrow a=0,2;b=0,4mol\\ n_{Fe}=2.0,2=0,4mol\\ n_{Cu}=n_{CuO}=0,4mol\\ m_{kl}=0,4\left(56+64\right)=48g\)

nO2 = 1,12/22,4 = 0,05 (mol)
PTHH: 3Fe + 2O2 -> (t°) Fe3O4
Mol: 0,075 <--- 0,05 ---> 0,025
mFe = 0,075 . 56 = 4,2 (g)
mFe3O4 = 0,025 . 232 = 5,8 (g)

a.\(n_{KMnO_4}=\dfrac{m_{KMnO_4}}{M_{KMnO_4}}=\dfrac{3,16}{158}=0,02mol\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,02 0,01 ( mol )
\(V_{O_2}=n_{O_2}.22,4=0,01.22,4=0,224l\)
b.
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
1/75 0,01 1/150 ( mol )
\(m_{Al}=n_{Al}.M_{Al}=\dfrac{1}{75}.27=0,36g\)
\(m_{Al_2O_3}=n_{Al_2O_3}.M_{Al_2O_3}=\dfrac{1}{150}.102=0,68g\)
2KMnO4-to>K2MnO4+MnO2+O2
0,02-------------------------------------0,01
4Al+3O2-to->2Al2O3
\(\dfrac{1}{75}\)---0,01---------\(\dfrac{1}{150}\)
n KMnO4=\(\dfrac{3,16}{158}\)=0,02 mol
=>VO2=0,01.22,4=0,224 l
b)m Al=\(\dfrac{1}{75}\).27=0,36g
=>m Al2O3=\(\dfrac{1}{150}\)102=0,68g

Áp dụng công thức Fa-ra-đây về điện phân, ta xác định được khoảng thời gian điện phân nhôm :
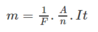
Thay số, ta có :
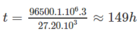
Điện năng tiêu thụ :
W = UIt = 5.20. 10 3 . 149.3600 = 5,364. 10 10 J
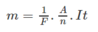

a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
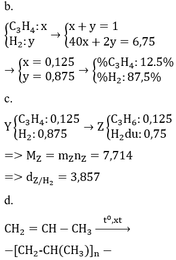


Đáp án B
+ Phản ứng thuận là tỏa nhiệt nên khi đun nóng cân bằng dịch trái (nhiệt độ giảm) → Số phân tử khí tăng → M giảm nên d2 < d1

MX = 3,17. 29 = 92 ⇒ 12x + y = 92 (1)
Gọi CTPT của X là CxHy:
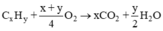
mCO2 = 4,28mH2O ↔ 44x = 4,28. 18. (y/2) ⇒ y = 1,14x (2)
Từ (1) và (2) ⇒ x = 7, y = 8. CTPT của X là C7H8
Từ đề bài ⇒ CTCT của X là:
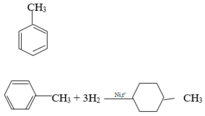
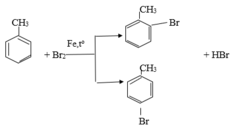
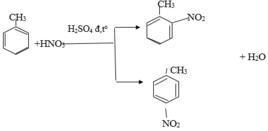
| Benzen | Hexen | Toluen | Eilen | |
| H2, xúc tác Ni | + | + | + | + |
| Br2 (dd) | + | + | ||
| Br2 có Fe, đun nóng | + | + | ||
| Dd KMnO4, nóng | + | + | + | |
| HBr | + | + | ||
| H2O(xt H+) | + | + |