Tìm khối lượng mỗi nguyên tố trong 24g Fe2O3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

tính phần trăm khối lượng của mỗi nguyên tố trong Fe2O3
tính khối lượng của mỗi nguyên tố trong Fe2O3

\(a.\%Fe=\dfrac{112}{160}=70\%\\ \%O=100\%-70\%=30\%\\ b.m_{Fe}=56.2=112\left(g\right)\\ m_O=16.3=48\left(g\right)\)

\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
Ta có: 80nCuO + 160nFe2O3 = 24 (1)
\(n_{H_2SO_4}=0,2.2=0,4\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{CuO}+3n_{Fe_2O_3}=0,4\left(2\right)\)
Từ (1) và (2) ⇒ nCuO = nFe2O3 = 0,1 (mol)
⇒ mCuO = 0,1.80 = 8 (g)
mFe2O3 = 0,1.160 = 16 (g)
\(n_{CuO}=a\left(mol\right);n_{Fe_2O_3}=b\left(mol\right)\left(a,b>0\right)\\ CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ \Rightarrow\left\{{}\begin{matrix}80a+160b=24\\a+3b=2.0,2=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \%m_{CuO}=\dfrac{0,1.80}{24}.100\%\approx33,333\%;\%m_{Fe_2O_3}=\dfrac{160.0,1}{24}.100\%\approx66,667\%\)

a) \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{20}{400}=0,05\left(mol\right)\)
=> \(\left\{{}\begin{matrix}n_{Fe}=0,1\left(mol\right)\\n_S=0,15\left(mol\right)\\n_O=0,6\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{Fe}=0,1.56=5,6\left(g\right)\\m_S=0,15.32=4,8\left(g\right)\\m_O=0,6.16=9,6\left(g\right)\end{matrix}\right.\)
b) \(n_{C_2H_6O}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
=> \(\left\{{}\begin{matrix}n_C=0,6\left(mol\right)\\n_H=1,8\left(mol\right)\\n_O=0,3\left(mol\right)\end{matrix}\right.\) => \(\left\{{}\begin{matrix}m_C=0,6.12=7,2\left(g\right)\\m_H=1,8.1=1,8\left(g\right)\\m_O=0,3.16=4,8\left(g\right)\end{matrix}\right.\)
c) Gọi số mol Fe2O3, MgO là a, b (mol)
=> 160a + 40b = 25
nO = 3a + b = \(\dfrac{25.32\%}{16}=0,5\) (mol)
=> a = 0,125 (mol); b = 0,125 (mol)
=> \(\left\{{}\begin{matrix}n_{Fe}=0,25\left(mol\right)\\n_{Mg}=0,125\left(mol\right)\\n_O=0,5\left(mol\right)\end{matrix}\right.\) => \(\left\{{}\begin{matrix}m_{Fe}=0,25.56=14\left(g\right)\\m_{Mg}=0,125.24=3\left(g\right)\\m_O=0,5.16=8\left(g\right)\end{matrix}\right.\)
a. Số mol sắt (III) sunfat Fe2(SO4)3 là 20/400=0,05 (mol).
mFe=0,05.2.56=5,6 (g), mS=0,05.3.32=4,8 (g), mO=0,05.3.4.16=9,6 (g).
b. Số mol khí C2H6O (ở đktc) là 6,72/22,4=0,3 (mol).
mC=0,3.2.12=7,2 (g), mH=0,3.6=1,8 (g), mO=0,3.16=4,8 (g).
c. Gọi x (mol) và y (mol) lần lượt là số mol của Fe2O3 và MgO.
160x+40y=25 (1).
\(\dfrac{3x.16+16y}{25}=32\%\) \(\Rightarrow\) 48x+16y=8 (2).
Giải hệ phương trình gồm (1) và (2), ta suy ra x=0,125 (mol) và y=0,125 (mol).
mFe=0,125.2.56=14 (g).
mMg=0,125.24=3 (g).
mO=(0,125.3+0,125).16=8 (g).

\(n_{MgO}=a\left(mol\right),n_{Fe_2O_3}=b\left(mol\right)\)
\(m_{hh}=40a+160b=24\left(g\right)\left(1\right)\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(n_{HCl}=2a+6b=1\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.2,b=0.1\)
\(m_{MgO}=0.2\cdot40=8\left(g\right)\)
\(m_{Fe_2O_3}=16\left(g\right)\)

Pt : \(CuO+2HCl\rightarrow CuCl_2+H_2O|\)
1 2 1 1
a 2a
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O|\)
1 6 2 3
b 6b
Gọi a là số mol của CuO
b là số mol của Fe2O3
\(m_{CuO}+m_{Fe2O3}=24\left(g\right)\)
⇒ \(n_{CuO}.M_{CuO}+n_{Fe2O3}.M_{Fe2O3}=24g\)
⇒ 80a + 160b = 24g (1)
Ta có : \(m_{Ct}=\dfrac{25.116,8}{100}=29,2\left(g\right)\)
\(n_{HCl}=\dfrac{29,2}{36,5}=0,8\left(mol\right)\)
⇒ 2a + 6b = 0,8(2)
Từ (1),(2) , ta có hệ phương trình :
80a + 260b = 24
2a + 6b = 0,4
⇒ \(\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
\(m_{CuO}=0,1.80=8\left(g\right)\)
\(m_{Fe2O3}=0,1.160=16\left(g\right)\)
0/0CuO = \(\dfrac{8.100}{24}=33,33\)0/0
0/0Fe2O3 = \(\dfrac{16.100}{24}=66,67\)0/0
Chúc bạn học tốt

PTHH: Fe2O3 + 3 H2 -to-> 2 Fe +3 H2O
x____________3x_______2x(mol)
CuO + H2 -to-> Cu + H2O
y___y________y(mol)
Hệ pt:
\(\left\{{}\begin{matrix}160x+80y=24\\3x+y=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
-> mCuO= 0,1.80=8(g)
-> %mCuO=(8/24).100 \(\approx\) 33,333%
-> %mFe2O3 \(\approx\) 66,667%
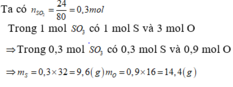
\(n_{Fe_2O_3}=\dfrac{24}{160}=0,15\left(mol\right)\)
=> \(n_{Fe}=0,3\left(mol\right);n_O=0,45\left(mol\right)\)
=> \(m_{Fe}=16,8\left(g\right);m_O=7,2\left(g\right)\)