trong 1 bình kín dung tích 16 lít chứa hỗn hợp CO , CO2 và O2 dư . thể tích O2 nhiều gấp đôi thể tích CO . bật tia lửa điện để đốt cháy hoàn toàn hỗn hợp , thể tích khí trong bình giảm 2 lít (các thể tích khí trong bình được đo ở cùng điều kiện nhiệt độ và áp suất ) . thành phần % theo thể tích CO , CO2 và O2 trong hỗn hợp ban đầu là bao nhiêu ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : C
Vì phản ứng cháy không cho biết có hoàn toàn hay không :
(*) TH1 : Lượng khí thoát ra chính là O2 dư => nO2 pứ = 0,05 mol
, nCaCO3 = 0,03 mol ; nCa(OH)2 = 0,035 mol
+) Nếu OH dư => nCO2 = nCaCO3 = 0,03 mol
Bảo toàn O : 2nO2 = 2nCO2 + nH2O => nH2O = 0,04 mol
=> nC : nH = 0,03 : 0,08 = 3 : 8 => C3H8
+) Nếu có HCO3- => nCaCO3 = nCO3 = nOH – nCO2 => nCO2 = 0,04 mol
Bảo toàn O => nH2O = 0,02
=> nC: nH = 0,04 : 0,04 = 1 : 1 => C2H2 hoặc C4H4
(*) TH2 : Hydrocacbon chưa cháy hết và 2,24 lit khí thoát ra chính là A
+) Nếu OH dư => nCO2 = nCaCO3 = 0,03 mol
Bảo toàn O : 2nO2 = 2nCO2 + nH2O => nH2O = 0,06 mol
=> nC : nH = 0,03 : 0,12 = 1 : 4 => CH4
+) Nếu có HCO3- => nCaCO3 = nCO3 = nOH – nCO2 => nCO2 = 0,04 mol
Bảo toàn O => nH2O = 0,04
=> nC: nH = 0,04 : 0,084 = 1 : 2 => C2H4 ; C3H6 hoặc C4H8
Tổng cộng có 7 chất thỏa mãn

Đáp án A
Do điều kiện như nhau nên ta sử dụng thể tích như số mol (để tiện tính toán)
Ta có: 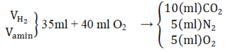
Amin đơn chức ⇒ Vamin = 2 V N 2 = 10 ml
⇒ V H 2 = 35 – 10 = 25 ml
⇒ Số C của amin là: V C O 2 V a m i n = 10 10 = 1
Trong các phương án đã cho chỉ có CH5N thỏa mãn

