tiến hành điện phân 500ml dd nacl 4M ( D=1,12 g/ml). sau 75% nacl bị điện phân thì dừng lại. tính nòng độ % của các chất sau điện phân
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đổi : 500ml = 0,5 l
n NaCl = 4 . 0,5 = 2 mol
\(\Rightarrow\) m NaCl bị điện phân = 2 . 75% = 1,5 mol
2NaCl + 2H2O \(\rightarrow\) 2NaOH + H2 + Cl2
1,5............................1,5........0,75.....075
m dd NaCl = 500 . 1,2 = 600 g
m dd sau pứ = m dd NaCl - m H2 - m Cl2
= 600 - 0,75 . 2 - 0,75 . 71 = 545,25 g
m NaOH = 0,75 . 40 = 30 g
C% NaOH = \(\dfrac{30}{545,25}\).100% = 5,5 %

Chọn đáp án B
Ta có:
![]()
![]()
BTNT.Clo → Khí thoát ra ở cực dương phải là Cl2 và O2 .
Ta có
![]()
![]()
Và
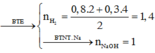
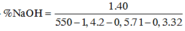
=7,96%

\(n_{NaCl} = 0,5.0,1 = 0,05(mol); n_{AlCl_3} = 0,5.0,3 = 0,15(mol)\)
2AlCl3 + 6H2O → 2Al(OH)3 + 3H2 + 3Cl2
0,15..........................0,15.................................(mol)
2NaCl + 2H2O → 2NaOH + H2 + Cl2
0,05.........................0,05.........................(mol)
Al(OH)3 + NaOH → NaAlO2 + 2H2O
0,05............0,05.....................................(mol)
\(n_{Al(OH)_3} = 0,15 - 0,05 =0,1(mol)\\ 2Al(OH)_3 \xrightarrow{t^o} Al_2O_3 + 3H_2O\\ n_{Al_2O_3} = \dfrac{1}{2}n_{Al(OH)_3} = 0,05(mol)\\ m_{Al_2O_3} = 0,05.102 = 5,1(gam)\)

Chọn A.
Khi cho Fe tác dụng với Y thì hỗn hợp rắn gồm Cu và Fe dư.
với nFe pư =
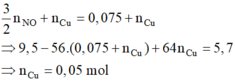
và n H + = 4 n NO = 0 , 2 mol . Dung dịch Y gồm Cu2+ (0,05); H+ (0,2); Na+ (0,5V) và NO3- (2V)
→ BTDT V = 0,2. Dung dịch ban đầu gồm Cu(NO3)2 (0,2 mol) và NaCl (0,1 mol)
Khối lượng dung dịch giảm: m = 64.(0,2 - 0,05) + 71.0,05 + 32.0,05 = 14,75 (g)




