hoà tan hết 5,6 g Fe trong dung dịch H2SO4 đặc nóng dư .Thu được V lít SO2(đktc). hấp thụ hết lượng khí này trong 100 ml dung dịch chứa đồng thời NaOH 0,1 M và Ba(OH)2 1,2M .thu được m gam kết tủa .Tính m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
Ta có: n F e 3 O 4 = 0,16 mol; n B a C O 3 = 0,22 mol
CO + Fe3O4→ Hỗn hợp rắn X có chứa Fe, FeO, Fe3O4+ H2SO4 đặc nóng→ SO2
Bản chất phản ứng:
CO + O oxit → CO2
CO2+ Ba(OH)2→ BaCO3+ H2O
nCO = n C O 2 = n B a C O 3 = 0,22 mol
- Quá trình cho electron:
Fe3O4 → 3Fe+3+ 1e
C+2 → C+4+ 2e
Tổng số mol e cho là: ne cho = n F e 3 O 4 + 2.nCO = 0,16+ 2.0,22 = 0,6 mol
- Quá trình nhận electron:
S+6+ 2e → SO2
Theo bảo toàn electron: ne cho = ne nhận = 0,6 mol
→ n S O 2 = 0,3 mol → V = 6,72 lít

H2SO4 dùng dư đề cho rõ ràng nhé → 21,4 gam kết tủa rõ là 0,2 mol Fe(OH)3.
mà có 0,9 mol NaOH → chứng tỏ nH+ trong Y = 0,3 mol. hết.!
(p/s: đừng nhầm lẫn 0,2 mol Fe(OH)3 → ∑nFe trong X = 0,2 luôn nhé.!).
♦ CB3: 19,2 gam (Fe; O) + 0,75 mol H2SO4 (lượng đủ) → Fe2(SO4)3 + SO2 + H2O.
có 2x mol Fe → x mol Fe2(SO4)3
→ nSO2 = 0,75 – 3x theo bảo toàn S.
bảo toàn electron có 2nO trong X = 3nFe – 2nSO2
→ nO trong X = 6x – 0,75 mol
||→ mX = mFe + mO = 56 × 2x + 16 × (6x – 0,75) = 19,2
→ giải ra: x = 0,15 mol.
→ nSO2 = 0,75 – x = 0,3 mol → Yêu cầu VSO2 = 6,72 lít.
p/s: giải CB3 có khá nhiều hướng khác: ví dụ gọi x như trên thì có SO2 theo x;
nH2O = 0,375 mol → BTKL cả phương trình giải ra x luôn.!
Đáp án B

Bảo toàn electron: \(n_{SO_2}=n_{FeO}:2=0,2:2=0,1mol\)
Nhận thấy \(1< n_{OH}:n_{SO2}=0,13:0,1< 2\Rightarrow\) tạo đồng thời muối trung hòa và muối axit
\(SO_2+OH\rightarrow SO_3^{2-}+H_2O\)
\(X\Rightarrow2X\)
\(SO_2+OH\rightarrow HSO_3\)
\(y\Rightarrow y\)
Ta có hệ:\(\left\{{}\begin{matrix}x+y=0,1\\2x+y=0,13\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}x=0,03\\y=0,07\end{matrix}\right.\)
Dung dịch sau phản ứng chứa: \(Na^+:0,06mol,K^+:0,07mol,SO_3^{2-}:0,03mol,HSO_3:0,07mol\)
Vậy \(m_{muối}=m_{Na^+}+m_{K^+}+m_{SO_3^{2-}}+m_{HSO_3}=12,18gam\)



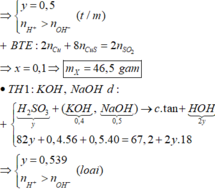

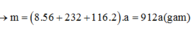
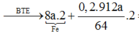
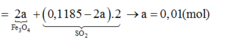


PTHH: \(2Fe+6H_2SO_4\left(đăc\right)\underrightarrow{t^o}Fe_2\left(SO4\right)_3+3SO_2+6H_2O\)
nFe = 5,6 / 56 = 0,1 (mol)
=> nSO2 = 0,15 (mol)
nNaOH = 0,1 x 0,1 = 0,01 (mol)
=> nOH- = 0,01 (mol)
nBa(OH)2 = 1,2 x 0,1 = 0,12 (mol)
=> nOH- = 0,24 (mol)
=> \(\sum n_{OH^-}=0,24+0,01=0,25\left(mol\right)\)
Ta có: \(1< \frac{n_{OH^-}}{n_{SO2}}< 2\)
=> Phản ứng tạo 2 muối.
Ta có phương trình ion sau:
SO22- + 2OH- ===> SO32- + H2O (1)
a...............2a
SO22- + OH- ===> HSO3- (2)
b..............b
Đặt nSO2 ở phản ứng (1), (2) lần lượt là a, b
Ta có hệ phương trình:
\(\begin{cases}a+b=0,15\\2a+b=0,25\end{cases}\)
\(\Rightarrow\begin{cases}a=0,1\\b=0,05\end{cases}\)
Lượng kết tủa là BaCO3
=> m = 0,1 x 217 = 21,7 gam