Tính khối lượng kết tủa tạo thành khi trộn lẫn dd chứa 0,63g NaHCO3 với dd chứa 1,71g Ba(OH)2.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$n_{NaHCO_3} = \dfrac{1,26}{84}= 0,015(mol)$
$n_{Ca(OH)_2} = \dfrac{1,48}{74} = 0,02(mol)$
Ta thấy : $n_{NaHCO_3} < n_{Ca(OH)_2$ nên PTHH là :
$NaHCO_3 + Ca(OH)_2 \to NaOH + CaCO_3 + H_2O$
Theo PTHH :
$n_{CaCO_3} = n_{NaHCO_3} = 0,015(mol)$
$m_{CaCO_3} = 0,015.100 = 1,5(gam)$

PTHH: \(2NaHCO_3+Ca\left(OH\right)_2\rightarrow Na_2CO_3+CaCO_3\downarrow+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{NaHCO_3}=\dfrac{1,26}{84}=0,015\left(mol\right)\\n_{Ca\left(OH\right)_2}=\dfrac{1,48}{74}=0,02\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,015}{2}< \dfrac{0,02}{1}\) \(\Rightarrow\) Ca(OH)2 còn dư
\(\Rightarrow n_{CaCO_3}=\dfrac{1}{2}n_{NaHCO_3}=0,0075\left(mol\right)\) \(\Rightarrow m_{CaCO_3}=100\cdot0,0075=0,75\left(g\right)\)

đang cần gấp ai lm đc gúp em trong chiều nay đc ko ạ cảm ơn nhìu nhìu
\(n_{NaHCO_3}=\dfrac{0,63}{84}=0,0075\left(mol\right);n_{Ba\left(OH\right)_2}=\dfrac{1,71}{171}=0,01\left(mol\right)\)
PTHH: 2NaHCO3 + Ba(OH)2 → BaCO3 + Na2CO3 + 2H2O
Mol: 0,0075 0,00375
Ta có:\(\dfrac{0,0075}{2}< \dfrac{0,01}{1}\)⇒NaHCO3 pứ hết, Ba(OH)2 dư
⇒ \(m_{BaCO_3}=0,00375.197=0,73875\left(g\right)\)
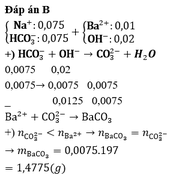
nNaHCO3 = 0,0075
nBa(OH)2 = 0,01 mol
Pt: HCO3- + OH- -> CO3 + H2O
0,0075------------> 0,0075
mBaCO3 = 1,4775g