Câu 1: Thực hiện phản ứng giữa H2 và N2 (tỉ lệ mol 4:1), trong bình kín có xúc tác, thu được hỗn hợp khí có áp suất giảm 9% so với ban đầu ( trong cùng điều kiện). Tính Hiệu suất phản ứng.
Câu 2: Trộn 3 dung dịch HCl 0,3M; H2SO4 0,2M; và H3PO4 0,1M với những thể tích bằng nhau thu được dung dịch A. Để trung hòa 300ml dung dịch A cần vừa đủ V ml dung dịch B gồm NaOH 0,2M và Ba(OH)2 0,1M. Tính giá trị của V.
Câu 3: Hòa tan hoành toàn m gam Al trong dung dịch HNO3, thấy tạo ra 4,48 lít hỗn hợp 3 khí NO, N2, N2O (tỉ lệ mol nNO : nN2 : nN2O = 1:2:2) Thể tích dung dịch HNO3 1M cần bao nhiêu lít?



 A.
A.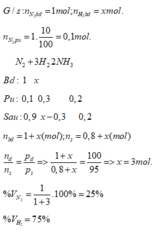
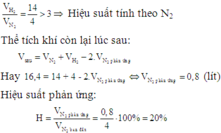
Câu 3: Gọi số mol NO là a . Có: n\(_{N_2}\) = n\(_{N_2O}\) = 2a => 5a = \(\dfrac{4,48}{22,4}\) = 0,2
=> a = 0,04 . Vậy: n\(HNO_3\) = a.4+2a.10+2a.12 = 1,92 (mol)
=> V\(_{HNO_3}\) = 1,92 (lít)