hòa tan hoàn toàn hỗn hợp gồm fe, al bằng dung dịch H2SO4 loãng thu dược 10,08 l H2 đkc. mặt khác nếu cũng cho lương hỗn hợp trên phản ứng với dung dịch KOH thì thu được 6,72 l H2 đtc. tính mAl, mFe
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

25 tháng 3 2018
Đáp án : A
nH2 = 0,25 mol; nSO2 = 0,3 mol
2H+ + 2e → H2 S+6 + 2e → S+4
0,5 <-- 0,25 0,6 <-- 0,3
nFe = 0,6 – 0,5 = 0,1 mol
=> mFe = 5,6g

H
7 tháng 4 2021
\(Mg + H_2SO_4 \to MgSO_4 + H_2\\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ Zn + H_2SO_4 \to ZnSO_4 + H_2\\ n_{H_2} = n_{H_2SO_4} = a(mol)\\ \text{Bảo toàn khối lượng : }\\ 20 + 98a = 58,4 + 2a\\ \Rightarrow a = 0,4\\ \Rightarrow V_1 = \dfrac{0,4}{0,5} = 0,8(lít) = 800(ml)\\ V_2 = 0,4.22,4 = 8,96(lít)\)
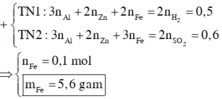



Fe + H2SO4 → FeSO4 + H2 (1)
2Al + 3H2SO4→Al2(SO4)3+3H2 (2)
nH2(1),(2)=10,08:22,4=0,45 mol
nH2(3)=6,72:22,4=0,3 mol
mặt khác ta có phương trình:2 KOH+2Al+2H2O→2KAlO2+3H2(3)
0,2mol<---------------------- 0,3mol
→ mAl= 0,2. 27=5,4 g
theo phương trình (2) có: nH2(2)=3/2 nAl=3/2 . 0,2 = 0,3 mol
→ nH2(1)=nH2(1),(2) - nH2(2)=0,45-0,3= 0,15 mol
theo pt (1) có: nFe=n H2(1)=0,15 mol→mFe=0,15. 56=8,4g