Đốt cháy 4,96g photpho trong không khí thu được 8g P2O5 . Tính hiệu suất của phản ứng trên
Help tớ vs , tớ ko biết j về hiệu suất hết !!
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_3PO_4}=\dfrac{9,8}{98}=0,1(mol)\\ PTHH:4P+5O_2\xrightarrow{t^o}2P_2O_5\\ P_2O_5+3H_2O\to 2H_3PO_4\\ \Rightarrow n_{P}=2n_{P_2O_5}=n_{H_3PO_4}=0,1(mol)\\ \Rightarrow m_{P(phản ứng)}=0,1.31=3,1(g)\\ \Rightarrow H\%=\dfrac{3,1}{7,75}.100\%=40\%\)

a)
\(n_{P_2O_5} = \dfrac{42,6}{142} = 0,3(mol)\\ \)
4P + 5O2 \(\xrightarrow{t^o}\) 2P2O5
0,6.............0,75.................0,3..........(mol)
mP = 0,6.31 = 18,6(gam)
b)
2KClO3 \(\xrightarrow{t^o}\) 2KCl + 3O2
0,5....................................0,75.....(mol)
\(m_{KClO_3} = 0,5.122,5 = 61,25(gam)\)
c)
\(3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\)
\(n_{Fe} = \dfrac{16,8}{56} = 0,3(mol)\\ \dfrac{n_{Fe}}{3} = 0,1 < \dfrac{n_{O_2}}{2} = 0,375\)
nên hiệu suất tính theo số mol Fe.
\(n_{Fe\ pư} = 0,3.90\% = 0,27(mol)\\ n_{Fe_3O_4} =\dfrac{1}{3}n_{Fe\ pư} = 0,09(mol)\\ \Rightarrow m_{Fe_3O_4} = 0,09.232 = 20,88(gam)\)

\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
PT: \(4Na+O_2\underrightarrow{t^o}2Na_2O\)
Theo PT: \(n_{Na_2O\left(LT\right)}=\dfrac{1}{2}n_{Na}=0,1\left(mol\right)\)
\(\Rightarrow m_{Na_2O\left(LT\right)}=0,1.62=6,2\left(g\right)\)
\(\Rightarrow H=\dfrac{4,96}{6,2}.100\%=80\%\)

\(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:4P+5O_2\underrightarrow{t^o}2P_2O_5\\ LTL:\dfrac{0,2}{4}< \dfrac{0,4}{5}\Rightarrow O_2dư\)
\(n_{O_2\left(pư\right)}=\dfrac{5}{4}n_P=\dfrac{5}{4}.0,2=0,25\left(mol\right)\\ n_{O_2\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(n_{P_2O_5\left(lt\right)}=\dfrac{1}{2}n_P=\dfrac{1}{2}.0,2=0,1\left(mol\right)\\ m_{P_2O_5\left(lt\right)}=0,1.142=14,2\left(g\right)\\ m_{P_2O_5\left(tt\right)}=0,1.142.80\%=11,36\left(g\right)\)

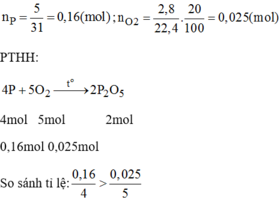
Vậy P dư nen tính bài toán theo n O 2
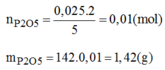
Khối lượng P 2 O 5 thực tế thu được: 1,42.80% = 1,136(g)

a) 4P + 5O2 --to--> 2P2O5
b) \(n_{P_2O_5}=\dfrac{34,08}{142}=0,24\left(mol\right)\)
4P + 5O2 --to--> 2P2O5
0,48<-0,6<------0,24
=> mO2 = 0,6.32 = 19,2 (g)
c)
C1: mP = 0,48.31 = 14,88(g)
C2:
Theo ĐLBTKL: mP + mO2 = mP2O5
=> mP = 34,08-19,2 = 14,88(g)
d)
VO2 = 0,6.22,4 = 13,44 (l)
=> Vkk = 13,44 :20% = 67,2 (l)
pt hh: 4P + 5O2 = 2P2O5
cứ 124g p thi thu dc 282g P2O5
vậy x g p...................8g...........
x = 124.8/282 = 3,5g p
hiệu suất là: η = (3,5 / 4,96 ).100% = 70%
nP = 4,96 / 31 = 0,16 mol
PTHH: 4P + 5O2 ===> 2P2O5
0,16 0,08 mol
Lập các số mol theo PTHH, ta có
nP2O5(phương trình) = 0,08 mol
=> mP2O5 ( phương trình) = 0,08 x 142 = 11,36 gam
Mà thực tế thu đc 8 gam P2O5
=> H = \(\frac{8}{11,36}.100\%\) = 70,42%