Lập CTPT của hợp chất A có % m các nguyên tố là 43,4% Na ; 11,3% C và O .Biết 0,2 mol A có k/lượng là 21,2 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) %Cl = 60,68%
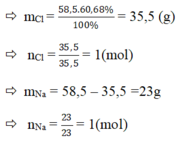
Vậy trong 1 phân tử hợp chất A có : 1 nguyên tử Na, 1 nguyên tử Cl.
⇒ CTHH của hợp chất A : NaCl
b)
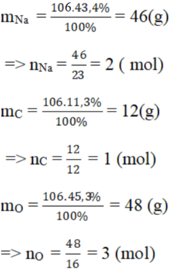
Vậy trong 1 phân tử hợp chất B có: 2 nguyên tử Na, 1 nguyên tử C, 3 nguyên tử O.
⇒ CTHH của hợp chất B : Na2CO3.

Đặt : CTHH có dạng là : \(Na_xC_yO_z\)
\(\%Na=\dfrac{23x}{106}\cdot100\%=43.4\%\)
\(\Rightarrow x=2\)
\(\%C=\dfrac{12x}{106}\cdot100\%=11.3\%\)
\(\Rightarrow y=1\)
\(z=\dfrac{106-23\cdot2-12}{16}=3\)
CTHH có dạng là : Na2CO3

bài1
ta có dA/H2=22 →MA=22MH2=22 \(\times\) 2 =44
nA=\(\frac{5,6}{22,4}\)=0,25
\(\Rightarrow\)mA=M\(\times\)n=11 g
MA=dA/\(H_2\)×M\(H_2\)=22×(1×2)=44g/mol
nA=VA÷22,4=5,6÷22,4=0,25mol
mA=nA×MA=0,25×44=11g

a) %m S = 12,9 %
n Ag : n S = \(\dfrac{87,1}{108}\div\dfrac{12,9}{32}\approx0,8\div0,4=2\div1\)
=> CTĐG : (Ag2S)n
Mà M Ag2S = 108 . 2 + 32 = 248 ( g / mol ) => n = 1
b) %m O = 53,33%
Có: n Mg : n S : n O = \(\dfrac{20}{24}\div\dfrac{26,67}{32}\div\dfrac{53,33}{16}=0,83\div0,83\div3,3\)
\(\approx1\div1\div4\)
=> CTĐG: (MgSO4)n
Mà M MgSO4 = 24 + 32 + 16 . 4 = 120 ( g / mol ) => n = 1
Vậy CT của B : MgSO4
c)
m K : m S : m O = 39 : 16 : 32
=> n K : n S : n O = 1 : 0,5 : 2 = 2 : 1 : 4
=> CT của D: K2SO4
d) Theo đề: M E = 2 . 28 = 56 ( g / mol )
%m H = 14,29 %
Có: n C : n H = \(\dfrac{85,71}{12}\div\dfrac{14,29}{1}=7,14\div14,29\approx1\div2\)
=> CTĐG : (CH2)n
Mà M CH2 = 12 + 2 = 14 ( g / mol ) => n = 4
Vậy Ct của E : C4H8
e) %m O = 46,21 %
n K : n Cl : n O = \(\dfrac{28,16}{39}\div\dfrac{25,63}{35,5}\div\dfrac{46,21}{16}=0,72\div0,72\div2,89\)
\(\approx1\div1\div4\)
=> CTĐG: ( KCLO4)n
Mà M KCLO4 = 39 + 35,5 + 16 . 4 = 138,5 ( g/mol )
=> n = 1
Vậy CT của F : KCLO4

a) Hợp chất A có khối lượng mol phân tử là 58,5 g/mol, thành phần các nguyên tố theo khối lượng: 60,68% Cl và còn lại là Na.
b) Hợp chất B có khối lượng mol phân tử là 106 g/mol, thành phần các nguyên tố theo khối lượng: 43,4% Na; 11,3% C; 45,3% O
Bài giải:
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl = = 35,5 đvC => nCl = 1 mol
=> MNa = = 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa = = 46 => nNa =
= 2 mol
MC = = 12 => nC = 1 mol
MO = = 48 => nO =
= 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl = = 35,5 đvC => nCl = 1 mol
=> MNa = = 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa = = 46 => nNa =
= 2 mol
MC = = 12 => nC = 1 mol
MO = = 48 => nO =
= 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3

MA = \(\frac{m}{n}=\frac{21,2}{0,2}=106\)(g/mol)
Ta có: Na chiếm 43,4% ; C chiếm 11,3% nên O chiếm 45,3%
Gọi CTHH của hợp chất là NaxCyZz
Khối lượng của mỗi nguyên tố có trong một mol hợp chất
mNa= \(\frac{106.43,4}{100}=46\left(g\right)\)
mC= \(\frac{106.11,3}{100}=12\left(g\right)\)
mO = \(\frac{106.45,3}{100}=48\left(g\right)\)
Số mol nguyên tử của mỗi nguyên tố có trong một mol hợp chất
nNa= \(\frac{m}{M}=\frac{46}{23}=2\left(mol\right)\)
mC=\(\frac{m}{M}=\frac{12}{12}=1\left(mol\right)\)
mO=\(\frac{m}{M}=\frac{48}{16}=3\left(mol\right)\)
Vậy CTHH của hợp chất là Na2CO3
BÀI NÀY CÓ NHIỀU CÁCH GIẢI NHA BẠN!
ta có MA = m : n =21,2 : 0,2 = 106 g/mol
%O = 100 - ( 43,4 + 11,3 ) = 45,3 %
ta có %Na : M Na ; %C : MC ; %O : MO
43,4 : 23 ; 11,3 : 12 ; 45,3 : 16
= 2 ; 1 ; 3
CTHH là Na2CO3