Đốt cháy hoàn toàn m gam chất A cần dùng 6,4g O2 (đktc) thu được 4,4 g CO2 (đktc) và 3,6 gam H2O .Tính m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Sơ đồ X + O 2 → C O 2 + H 2 O ( 1 )
Áp dụng định luật bảo toàn khối lượng cho sơ đồ (1), ta có :
m + m O 2 = m C O 2 + m H 2 O
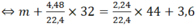
⇔ m = 1,6 gam

Sơ đồ: ( X ) + O 2 → C O 2 + H 2 O
Theo định luật bảo toàn khối lượng, ta có:
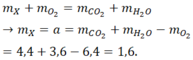

Sơ đồ: ( X ) + O 2 → C O 2 + H 2 O
Theo định luật bảo toàn khối lượng, ta có:


a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)

Chọn đáp án D
Quy đổi T về C (x mol), H (y mol), O (z mol). Bảo toàn C, H ta có sơ đồ phản ứng cháy sau:
T (C, H, O) + O2 → CO2 (x mol) + H2O (0,5y mol).
0,5y = 1,04 ⇒ y = 2,08.
Bảo toàn O ta có z + 1,6.2 = 2x + 0,5y ⇔ 2x – z = 2,16 (1).
Chất béo no có công thức chung là CnH2n–4O6.
ncbéo no = 1 6 nO = 1 6 z.
Nhận thấy: nC – 1 2 nH = 2ncbéo no ⇔ nH = 2x – 2 z 3 .
mcbéo no = 12x + 2x – 2 z 3 + 16z = 17,8 (2).
Từ (1) và (2) suy ra x = 1,14; z = 0,12.
Vậy x : y : z = 1,14 : 2,08 : 0,12 = 57 : 104 : 6 → T là C57H104O6.
MT = 884.

Chọn đáp án C
đốt x mol triglixerit T + 1,5 mol O2 → t 0 CO2 + 1,0 mol H2O.
Bảo toàn nguyên tố O có nCO2 = 3x + 1 mol.
Tương quan: nCO2 – nH2O = 3x = 3nT → ∑πtrong T = 3 + 1 = 4.
Mà sẵn trong T có 3πC=O → πC=C = 1 → 1T + 1H2 → 16,68 gam chất béo no.
||→ mT = 16,68 – 2x = 18 + 44 × (3x + 1) – 1,5 × 32 ||→ x = 0,02 mol.
Thay x ngược lại có mT = 16,64 gam → MT = Ans ÷ 0,02 = 832

\(V_{CO_2}=0,5.22,4=11,2\left(l\right)\)
\(A_{CO_2}=0,5.6.10^{23}=3.10^{23}\) (phân tử \(CO_2\) )
2.
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
=> \(n_C=n_{CO_2}=0,1\left(mol\right)\) (1)
=> \(n_O=2nCO_2=0,1.2=0,2\left(mol\right)\) (*)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
=> \(n_H=2n_{H_2O}=0,2.2=0,4\left(mol\right)\) (2)
=> \(n_O=n_{H_2O}=0,2\left(mol\right)\) (**)
\(n_{O_2}=\dfrac{4,8}{22,4}=0,2\left(mol\right)\)
=> \(n_O=2n_{O_2}=2.0,2=0,4\left(mol\right)\) (3)
\(X+O_2\underrightarrow{t^o}CO_2+H_2O\)
Từ (1),(2),(3), (*), (**) suy ra: \(n_C:n_H:n_O=0,1:0,4:0\)
=> Công thức tổng quát của X là \(C_xH_y\)
có: \(x:y=n_C:n_H=0,1:0,4=1:4\)
=> X là: \(CH_4\)
Sơ đồ pứ: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(m_{CH_4}=3,6+0,2.44-0,2.32=6\left(g\right)\)

Chọn đáp án A
♦ giải đốt m gam E O 2 + 0 , 1125 m o l O 2 → t 0 0 , 1 m o l C O 2 + 0 , 075 m o l H 2 O
E là este đơn chức → E có 2O
→ bảo toàn O có n E = 0 , 025 m o l
→ CTPT của E là C 4 H 6 O 2
→ E là este đơn chức, mạch hở, có 1 nối đôi C=C
Mà ancol tạo este no nên gốc hiđrocacbon của axit chứa nối đôi C=C này.
→ CTCT của E là C H 2 = C H C O O C H 3 → ancol Y là C H 3 O H

Bảo toàn khối lượng: \(m_A=m_{CO_2}+m_{H_2O}-m_{O_2}=1,6\left(g\right)\)